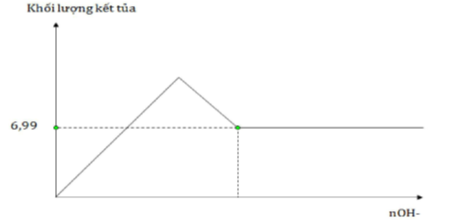
Câu hỏi: Nhỏ từ từ dung dịch đến dư Ba(OH)2 0,2M vào 100 ml dung dịch A chứa Al2(SO4)3 x M. Mối quan hệ giữa khối lượng kết tủa và số mol OH- được biểu diễn bằng đồ thị sau:
Nếu cho 100ml dung dịch hỗn hợp Ba(OH)2 0,2M và NaOH 0,3M vào 100ml dung dịch A thì khối lượng kết tủa thu được là bao nhiêu?
A. 6,22 gam.
B. 5,70 gam.
C. 5,44 gam.
D. 4,66 gam.

Nếu cho 100ml dung dịch hỗn hợp Ba(OH)2 0,2M và NaOH 0,3M vào 100ml dung dịch A thì khối lượng kết tủa thu được là bao nhiêu?
A. 6,22 gam.
B. 5,70 gam.
C. 5,44 gam.
D. 4,66 gam.
Hướng dẫn giải:
+ Từ đồ thị ta thấy, khi cho thêm OH nhưng đồ thị đi ngang → ở giai đoạn này Al(OH)3 bị hòa tan hoàn toàn, kết tủa còn lại là BaSO4
→ mBaSO4 max = 6,99 (g) → nBaSO4 max = 6,99 : 233 = 0,03 (mol)
→ nSO42-bđ = 0,03 (mol) → nAl2(SO4)3 = 1/3.nSO42- = 0,03/3 = 0,01 (mol)
Vậy trong 100 ml dd A ban đầu chứa: nAl3+ = 0,02 (mol) và nSO42- = 0,03 (mol)
+Xét thí nghiệm,
nBa(OH)2 = 0,1,0,2 = 0,02 (mol); nNaOH = 0,1.0,3 = 0,03 (mol)
→ nBa2+ = 0,02 (mol) ; nOH- = 2nBa(OH)2 + nNaOH = 2.0,02 + 0,03 = 0,07 (mol)
Ta thấy: $\dfrac{{{n}_{O{{H}^{-}}}}}{{{n}_{A{{l}^{3+}}}}}=\dfrac{0,07}{0,02}=3,5\to $ xảy ra trường hợp tạo kết tủa Al(OH)3 cực đại sau đó kết tủa tan 1 phần
Ba2+ + SO42- → BaSO4
3OH- + A13+ → Al(OH)3↓
OH- + Al(OH)3 → A1O2- + 2H2O
nBaSO4 = nBa2+ = 0,02 (mol) (Vì SO42- dư)
áp dụng công thức nhanh ta có: nOH- = 4nAl3+ = nAl(OH)3 + nAl(OH)3 = 4.0,02 – 0,07 = 0,01 (mol)
→ m↓ = mBaSO4 + mAl(OH)3 = 0,02. 233 + 0,01.78 = 5,44 (g)
+ Từ đồ thị ta thấy, khi cho thêm OH nhưng đồ thị đi ngang → ở giai đoạn này Al(OH)3 bị hòa tan hoàn toàn, kết tủa còn lại là BaSO4
→ mBaSO4 max = 6,99 (g) → nBaSO4 max = 6,99 : 233 = 0,03 (mol)
→ nSO42-bđ = 0,03 (mol) → nAl2(SO4)3 = 1/3.nSO42- = 0,03/3 = 0,01 (mol)
Vậy trong 100 ml dd A ban đầu chứa: nAl3+ = 0,02 (mol) và nSO42- = 0,03 (mol)
+Xét thí nghiệm,
nBa(OH)2 = 0,1,0,2 = 0,02 (mol); nNaOH = 0,1.0,3 = 0,03 (mol)
→ nBa2+ = 0,02 (mol) ; nOH- = 2nBa(OH)2 + nNaOH = 2.0,02 + 0,03 = 0,07 (mol)
Ta thấy: $\dfrac{{{n}_{O{{H}^{-}}}}}{{{n}_{A{{l}^{3+}}}}}=\dfrac{0,07}{0,02}=3,5\to $ xảy ra trường hợp tạo kết tủa Al(OH)3 cực đại sau đó kết tủa tan 1 phần
Ba2+ + SO42- → BaSO4
3OH- + A13+ → Al(OH)3↓
OH- + Al(OH)3 → A1O2- + 2H2O
nBaSO4 = nBa2+ = 0,02 (mol) (Vì SO42- dư)
áp dụng công thức nhanh ta có: nOH- = 4nAl3+ = nAl(OH)3 + nAl(OH)3 = 4.0,02 – 0,07 = 0,01 (mol)
→ m↓ = mBaSO4 + mAl(OH)3 = 0,02. 233 + 0,01.78 = 5,44 (g)
Đáp án C.