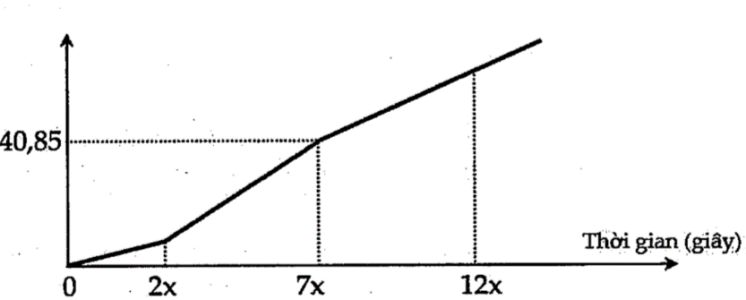
Câu hỏi: Hòa tan hoàn toàn hỗn hợp X gồm ba chất $FeC{{l}_{3}},FeC{{l}_{2}},CuC{{l}_{2}}$ trong nước thu được dung dịch Y. Điện phân dung dịch Y bằng dòng điện một chiều với điện cực trơ. Đồ thị biểu diễn khối lượng dung dịch giảm theo thời gian như sau:
Nếu cho NaOH dư vào dung dịch đã điện phân được 10x giây thì thu được 31,5 gam kết tủa. Nếu điện phân dung dịch Y trong 12x giây sau đó cho $AgN{{O}_{3}}$ dư vào dung dịch sau điện phân thì khối lượng kết tủa thu được gần nhất với:
A. 100
B. 99
C. 180
D. 179

Nếu cho NaOH dư vào dung dịch đã điện phân được 10x giây thì thu được 31,5 gam kết tủa. Nếu điện phân dung dịch Y trong 12x giây sau đó cho $AgN{{O}_{3}}$ dư vào dung dịch sau điện phân thì khối lượng kết tủa thu được gần nhất với:
A. 100
B. 99
C. 180
D. 179
Thứ tự điện phân bên catot: $F{{e}^{3+}};C{{u}^{2+}};F{{e}^{2+}}$ và bên anot có $C{{l}^{-}}$ bị điện phân.
Nhìn vào đồ thị ta thấy có 3 đoạn dung dịch thay đổi
+ Đoạn 1: bên catot chỉ có $F{{e}^{3+}}$ điện phân, anot có $C{{l}^{-}}$
+ Đoạn 2: bên catot có $F{{e}^{3+}}$ và $C{{u}^{2+}}$, anot có $C{{l}^{-}}$
+ Đoạn 3: bên catot có cả 3 ion điện phân, anot có $C{{l}^{-}}$
Tại 2x(s):
$F{{e}^{3+}}+1e\to F{{e}^{2+}}$ $2C{{l}^{-}}\to C{{l}_{2}}+2e$
Gọi $n\left( C{{l}^{-}} \right)=2a\to n\left( e \right)=n\left( F{{e}^{3+}}\text{ bd} \right)=2a\text{ mol}$
Tại 7x(s) thì n(e) = 7a (mol)
$\begin{aligned}
& F{{e}^{3+}}+1e\to F{{e}^{2+}} \\
& 2a\to 2a\to 2a \\
\end{aligned} $ $ \begin{aligned}
& 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& 7a\leftarrow 3,5a\leftarrow 7a \\
\end{aligned}$
$C{{u}^{2+}}+2e\to Cu$
$\to $ n(e trong đp $C{{u}^{2+}}$ )=5a $\to $ n( $C{{u}^{2+}}$ bđ)=2,5a (mol)
$\to $ m(dd giảm) = m(Cu) + m( $C{{l}_{2}}$ ) = 64.2,5a + 71.3,5a = 40,85 $\to $ a = 0,1 mol
Tại 10x(s) thì n(e)=1 mol
$\begin{aligned}
& F{{e}^{3+}}+1e\to F{{e}^{2+}} \\
& \text{0}\text{,2}\to 0,2\to 0,2 \\
\end{aligned} $ $ \begin{aligned}
& 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& \text{ 1 }\leftarrow 0,5\leftarrow 1 \\
\end{aligned}$
$\begin{aligned}
& C{{u}^{2+}}+2e\to Cu \\
& \text{0}\text{,25}\to 0,5\to 0,25 \\
\end{aligned}$
$F{{e}^{2+}}+2e\to Fe$
$\to $ n(e trong đp $F{{e}^{2+}}$ )=0,3 mol $\to $ n( $F{{e}^{2+}}$ đp)=0,15 mol
Dung dịch sau phản ứng có $F{{e}^{2+}}$ dư và $C{{l}^{-}}$
Kết tủa là $Fe{{\left( OH \right)}_{2}}\to n\left( Fe{{\left( OH \right)}_{2}} \right)=0,35mol$
$\to n\left( F{{e}^{2+}}\text{ d} \right)=n\left( F{{e}^{2+}}\text{ b} \right)+0,2-0,15=0,35mol$
$\to n\left( F{{e}^{2+}}\text{ b} \right)=0,3mol$
Vậy hỗn hợp ban đầu có: $FeC{{l}_{3}}:0,2mol;CuC{{l}_{2}}:0,25mol\text{ v }\!\!\mu\!\!\text{ }FeC{{l}_{2}}0,3mol$
Tại 12x(s): n(e)=1,2 mol
$\begin{aligned}
& F{{e}^{3+}}+1e\to F{{e}^{2+}} \\
& \text{0}\text{,2}\to 0,2\to 0,2 \\
\end{aligned} $ $ \begin{aligned}
& 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& \text{1}\text{,2 }\leftarrow 0,6\leftarrow 1,2 \\
\end{aligned}$
$\begin{aligned}
& C{{u}^{2+}}+2e\to Cu \\
& \text{0}\text{,25}\to 0,5\to 0,25 \\
\end{aligned}$
$\begin{aligned}
& F{{e}^{2+}}+2e\to Fe \\
& \text{0}\text{,25}\leftarrow 0,5\to 0,25 \\
\end{aligned}$
Dung dịch sau điện phân: $F{{e}^{2+}}\left( 0,3+0,2-0,25=0,25mol \right)$ và $C{{l}^{-}}\left( 0,5mol \right)$
Khi cho vào $AgN{{O}_{3}}$ thu được kết tủa gồm: Ag(0,25 mol) và AgCl(0,5 mol)
$\to $ m = 98,75 (gam)
Nhìn vào đồ thị ta thấy có 3 đoạn dung dịch thay đổi
+ Đoạn 1: bên catot chỉ có $F{{e}^{3+}}$ điện phân, anot có $C{{l}^{-}}$
+ Đoạn 2: bên catot có $F{{e}^{3+}}$ và $C{{u}^{2+}}$, anot có $C{{l}^{-}}$
+ Đoạn 3: bên catot có cả 3 ion điện phân, anot có $C{{l}^{-}}$
Tại 2x(s):
$F{{e}^{3+}}+1e\to F{{e}^{2+}}$ $2C{{l}^{-}}\to C{{l}_{2}}+2e$
Gọi $n\left( C{{l}^{-}} \right)=2a\to n\left( e \right)=n\left( F{{e}^{3+}}\text{ bd} \right)=2a\text{ mol}$
Tại 7x(s) thì n(e) = 7a (mol)
$\begin{aligned}
& F{{e}^{3+}}+1e\to F{{e}^{2+}} \\
& 2a\to 2a\to 2a \\
\end{aligned} $ $ \begin{aligned}
& 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& 7a\leftarrow 3,5a\leftarrow 7a \\
\end{aligned}$
$C{{u}^{2+}}+2e\to Cu$
$\to $ n(e trong đp $C{{u}^{2+}}$ )=5a $\to $ n( $C{{u}^{2+}}$ bđ)=2,5a (mol)
$\to $ m(dd giảm) = m(Cu) + m( $C{{l}_{2}}$ ) = 64.2,5a + 71.3,5a = 40,85 $\to $ a = 0,1 mol
Tại 10x(s) thì n(e)=1 mol
$\begin{aligned}
& F{{e}^{3+}}+1e\to F{{e}^{2+}} \\
& \text{0}\text{,2}\to 0,2\to 0,2 \\
\end{aligned} $ $ \begin{aligned}
& 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& \text{ 1 }\leftarrow 0,5\leftarrow 1 \\
\end{aligned}$
$\begin{aligned}
& C{{u}^{2+}}+2e\to Cu \\
& \text{0}\text{,25}\to 0,5\to 0,25 \\
\end{aligned}$
$F{{e}^{2+}}+2e\to Fe$
$\to $ n(e trong đp $F{{e}^{2+}}$ )=0,3 mol $\to $ n( $F{{e}^{2+}}$ đp)=0,15 mol
Dung dịch sau phản ứng có $F{{e}^{2+}}$ dư và $C{{l}^{-}}$
Kết tủa là $Fe{{\left( OH \right)}_{2}}\to n\left( Fe{{\left( OH \right)}_{2}} \right)=0,35mol$
$\to n\left( F{{e}^{2+}}\text{ d} \right)=n\left( F{{e}^{2+}}\text{ b} \right)+0,2-0,15=0,35mol$
$\to n\left( F{{e}^{2+}}\text{ b} \right)=0,3mol$
Vậy hỗn hợp ban đầu có: $FeC{{l}_{3}}:0,2mol;CuC{{l}_{2}}:0,25mol\text{ v }\!\!\mu\!\!\text{ }FeC{{l}_{2}}0,3mol$
Tại 12x(s): n(e)=1,2 mol
$\begin{aligned}
& F{{e}^{3+}}+1e\to F{{e}^{2+}} \\
& \text{0}\text{,2}\to 0,2\to 0,2 \\
\end{aligned} $ $ \begin{aligned}
& 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& \text{1}\text{,2 }\leftarrow 0,6\leftarrow 1,2 \\
\end{aligned}$
$\begin{aligned}
& C{{u}^{2+}}+2e\to Cu \\
& \text{0}\text{,25}\to 0,5\to 0,25 \\
\end{aligned}$
$\begin{aligned}
& F{{e}^{2+}}+2e\to Fe \\
& \text{0}\text{,25}\leftarrow 0,5\to 0,25 \\
\end{aligned}$
Dung dịch sau điện phân: $F{{e}^{2+}}\left( 0,3+0,2-0,25=0,25mol \right)$ và $C{{l}^{-}}\left( 0,5mol \right)$
Khi cho vào $AgN{{O}_{3}}$ thu được kết tủa gồm: Ag(0,25 mol) và AgCl(0,5 mol)
$\to $ m = 98,75 (gam)
Đáp án B.