Câu hỏi: Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2, thu được dung dịch X. Nhỏ rất từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ để các phản ứng xảy ra hoàn toàn. Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích dung dịch H2SO4 (V ml) như sau:
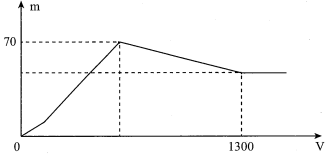
Giá trị của a là
A. 8,10
B. 4,05
C. 5,40
D. 6,75

Giá trị của a là
A. 8,10
B. 4,05
C. 5,40
D. 6,75
Xét Al + Ba(OH)2:
Gọi số mol Ba(OH)2 và Al lần lượt là x và y mol.
Sơ đồ phản ứng: $\underbrace{Al}_{y\ \text{mol}}+\underbrace{Ba{{(OH)}_{2}}}_{x\ mol}\to X\left\{ \begin{aligned}
& B{{a}^{2+}}:x\ mol \\
& AlO_{2}^{-}:y\ mol \\
& OH_{du}^{-} \\
\end{aligned} \right.$
Bảo toàn điện tích: ${{n}_{O{{H}^{-}}}}=2{{n}_{B{{a}^{2+}}}}-{{n}_{AlO_{2}^{-}}}=2\text{x}-y\text{ (mol)}$
Xét X + H2SO4:
Tại $V=1300$ ml hay ${{n}_{{{H}^{+}}}}=1,3\ mol$, Al(OH)3 bị hòa tan hết.
Ta có: ${{n}_{{{H}^{+}}}}=4{{n}_{AlO_{2}^{-}}}+{{n}_{O{{H}^{-}}}}\to 2\text{x}-y+4y=1,3$ (1)
Tại ${{m}_{\downarrow }}=70\ gam$, kết tủa cực đại gồm BaSO4 max và Al(OH)3.
Ta có: ${{n}_{{{H}_{2}}S{{O}_{4}}\ pu}}={{n}_{BaS{{O}_{4}}}}={{n}_{B{{a}^{2+}}}}=x\ mol\to {{n}_{{{H}^{+}}}}=2x\ mol$
$\to {{n}_{Al{{(OH)}_{3}}}}=\dfrac{4y-\left[ 2x-(2x-y) \right]}{3}=y\ mol\to 233x+78y=70$ (20
Từ (1) và (2) suy ra: $x=0,2;y=0,3\to {{m}_{Al}}=0,3.27=8,1\ gam$.
Gọi số mol Ba(OH)2 và Al lần lượt là x và y mol.
Sơ đồ phản ứng: $\underbrace{Al}_{y\ \text{mol}}+\underbrace{Ba{{(OH)}_{2}}}_{x\ mol}\to X\left\{ \begin{aligned}
& B{{a}^{2+}}:x\ mol \\
& AlO_{2}^{-}:y\ mol \\
& OH_{du}^{-} \\
\end{aligned} \right.$
Bảo toàn điện tích: ${{n}_{O{{H}^{-}}}}=2{{n}_{B{{a}^{2+}}}}-{{n}_{AlO_{2}^{-}}}=2\text{x}-y\text{ (mol)}$
Xét X + H2SO4:
Tại $V=1300$ ml hay ${{n}_{{{H}^{+}}}}=1,3\ mol$, Al(OH)3 bị hòa tan hết.
Ta có: ${{n}_{{{H}^{+}}}}=4{{n}_{AlO_{2}^{-}}}+{{n}_{O{{H}^{-}}}}\to 2\text{x}-y+4y=1,3$ (1)
Tại ${{m}_{\downarrow }}=70\ gam$, kết tủa cực đại gồm BaSO4 max và Al(OH)3.
Ta có: ${{n}_{{{H}_{2}}S{{O}_{4}}\ pu}}={{n}_{BaS{{O}_{4}}}}={{n}_{B{{a}^{2+}}}}=x\ mol\to {{n}_{{{H}^{+}}}}=2x\ mol$
$\to {{n}_{Al{{(OH)}_{3}}}}=\dfrac{4y-\left[ 2x-(2x-y) \right]}{3}=y\ mol\to 233x+78y=70$ (20
Từ (1) và (2) suy ra: $x=0,2;y=0,3\to {{m}_{Al}}=0,3.27=8,1\ gam$.
Đáp án A.