Câu hỏi: Hòa tan hoàn toàn 18,56 gam hỗn hợp gồm CuO, MgO và Al2O3 trong 400 ml dung dịch chứa H2SO4 0,4M và HCl 1,5M thu được dung dịch X. Cho từ từ dung dịch NaOH 1M vào X, sự phụ thuộc số mol kết tủa và thể tích dung dịch NaOH 1M được biểu diễn theo đề thị sau:
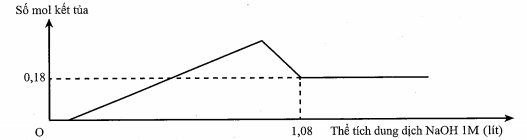
Nếu cho từ từ dung dịch chứa Ba(OH)2 0,2M và NaOH 1,2M vào dung dịch X, đến khi thu được khối lượng kết tủa lớn nhất, lọc kết tủa đem nung đến khối lượng không đổi, thu được m gam chất rắn khan. Giá trị của m là
A. 45,355.
B. 50,920.
C. 52,915.
D. 47,680.

Nếu cho từ từ dung dịch chứa Ba(OH)2 0,2M và NaOH 1,2M vào dung dịch X, đến khi thu được khối lượng kết tủa lớn nhất, lọc kết tủa đem nung đến khối lượng không đổi, thu được m gam chất rắn khan. Giá trị của m là
A. 45,355.
B. 50,920.
C. 52,915.
D. 47,680.
${{n}_{{{H}_{2}}S{{O}_{4}}}}=0,16 mol$ ; ${{n}_{HCl}}=0,6 mol\to {{n}_{{{H}^{+}}}}=0,92 mol$
Gọi số mol của CuO, MgO và Al2O3 lần lượt là a, b và c mol.
$\to 80a+40b+102c=18,56$ $\left( 1 \right)$
Xét X tác dụng với dung dịch NaOH:
Tạo ${{n}_{NaOH}}=1,08 mol$, kết tủa thu được gồm Cu(OH)2 và Mg(OH)2; Al(OH)3 đã đạt cực đại và bị hòa tan hết.
$\to a+b=0,18$ $\left( 2 \right)$
Ta có: ${{n}_{NaOH}}={{n}_{{{H}^{+}}du}}+2{{n}_{C{{u}^{2+}}}}+2{{n}_{M{{g}^{2+}}}}+4{{n}_{A{{l}^{3+}}}}$
$\Leftrightarrow \left[ 0,92-2\left( a+b+3c \right) \right]+2a+2b+4.2c=1,08\to c=0,08$ $\left( 3 \right)$
Từ $\left( 1 \right)$, $\left( 2 \right)$ và $\left( 3 \right)$ suy ra: $a=0,08$ ; $b=0,1$ ; $c=0,08$
→ Dung dịch X gồm Cu2+ (0,08 mol); Mg2+ (0,1 mol); Al3+ (0,16 mol); H+ dư (0,08 mol); $SO_{4}^{2-}$ (0,16 mol) và Cl– (0,6 mol).
Xét X tác dụng với Ba(OH)2 và NaOH:
TH 1: Al(OH)3 kết tủa cực đại.
Gọi số mol Ba(OH)2 và NaOH phản ứng lần lượt là x và 6x mol.
Ta có: ${{n}_{O{{H}^{-}}}}=2{{n}_{SO_{4}^{2-}}}+{{n}_{C{{l}^{-}}}}\Leftrightarrow 2x+6x=0,92\to x=0,115 mol$
Ta thấy: ${{n}_{B{{a}^{2+}}}}<{{n}_{SO_{4}^{2-}}}\to {{n}_{\text{BaS}{{O}_{4}}}}={{n}_{B{{a}^{2+}}}}=0,115 mol$
Kết tủa gồm Cu(OH)2 (0,08 mol); Mg(OH)2 (0,1 mol); Al(OH)3 (0,16 mol) và BaSO4 (0,115 mol).
$\to {{m}_{kết\ tủa}}=0,08.98+0,1.58+0,16.78+0,115.233=52,915gam$
TH 2: BaSO4 kết tủa cực đại.
${{n}_{Ba{{\left( OH \right)}_{2}}}}={{n}_{BaS{{O}_{4}}}}=n_{SO_{4}^{2-}}^{{}}=0,16 mol\to {{n}_{NaOH}}=0,16.6=0,96 mol$
Ta có: ${{n}_{O{{H}^{-}}}}=1,28 mol>1,08\to $ Al(OH)3 đã bị hòa tan hết
Kết tủa gồm Cu(OH)2 (0,08 mol); Mg(OH)2 (0,1 mol) và BaSO4 (0,16 mol).
$\to {{m}_{kết\ tủa}}=0,08.98+0,1.58+0,16.233=50,92 gam$
Nhận xét: ${{m}_{kết\ tủa\left( TH2 \right)}}<{{m}_{kết\ tủa\left( TH1 \right)}}\to $ Loại TH2.
→ m gam chất rắn khan gồm CuO, MgO, Al2O3 và BaSO4.
Do số mol Cu, Mg, AI được bảo toàn nên ${{m}_{CuO}}+{{m}_{MgO}}+{{m}_{A{{l}_{2}}{{O}_{3}}}}=18,56 gam$
$\to m=18,56+0,115.233=45,355 gam$
Chú ý: Đề bài hỏi tại thời điểm kết tủa thu được là lớn nhất, nếu đem nung két tủa đó thu được bao nhiêu gam chất rắn khan. Tránh nhầm lẫn với:
Trường hợp tìm giá trị lớn nhất của m → Chọn nhầm đáp án D.
Trường hợp tìm khối lượng kết tủa lớn nhất → Chọn nhầm đáp án C.
Gọi số mol của CuO, MgO và Al2O3 lần lượt là a, b và c mol.
$\to 80a+40b+102c=18,56$ $\left( 1 \right)$
Xét X tác dụng với dung dịch NaOH:
Tạo ${{n}_{NaOH}}=1,08 mol$, kết tủa thu được gồm Cu(OH)2 và Mg(OH)2; Al(OH)3 đã đạt cực đại và bị hòa tan hết.
$\to a+b=0,18$ $\left( 2 \right)$
Ta có: ${{n}_{NaOH}}={{n}_{{{H}^{+}}du}}+2{{n}_{C{{u}^{2+}}}}+2{{n}_{M{{g}^{2+}}}}+4{{n}_{A{{l}^{3+}}}}$
$\Leftrightarrow \left[ 0,92-2\left( a+b+3c \right) \right]+2a+2b+4.2c=1,08\to c=0,08$ $\left( 3 \right)$
Từ $\left( 1 \right)$, $\left( 2 \right)$ và $\left( 3 \right)$ suy ra: $a=0,08$ ; $b=0,1$ ; $c=0,08$
→ Dung dịch X gồm Cu2+ (0,08 mol); Mg2+ (0,1 mol); Al3+ (0,16 mol); H+ dư (0,08 mol); $SO_{4}^{2-}$ (0,16 mol) và Cl– (0,6 mol).
Xét X tác dụng với Ba(OH)2 và NaOH:
TH 1: Al(OH)3 kết tủa cực đại.
Gọi số mol Ba(OH)2 và NaOH phản ứng lần lượt là x và 6x mol.
Ta có: ${{n}_{O{{H}^{-}}}}=2{{n}_{SO_{4}^{2-}}}+{{n}_{C{{l}^{-}}}}\Leftrightarrow 2x+6x=0,92\to x=0,115 mol$
Ta thấy: ${{n}_{B{{a}^{2+}}}}<{{n}_{SO_{4}^{2-}}}\to {{n}_{\text{BaS}{{O}_{4}}}}={{n}_{B{{a}^{2+}}}}=0,115 mol$
Kết tủa gồm Cu(OH)2 (0,08 mol); Mg(OH)2 (0,1 mol); Al(OH)3 (0,16 mol) và BaSO4 (0,115 mol).
$\to {{m}_{kết\ tủa}}=0,08.98+0,1.58+0,16.78+0,115.233=52,915gam$
TH 2: BaSO4 kết tủa cực đại.
${{n}_{Ba{{\left( OH \right)}_{2}}}}={{n}_{BaS{{O}_{4}}}}=n_{SO_{4}^{2-}}^{{}}=0,16 mol\to {{n}_{NaOH}}=0,16.6=0,96 mol$
Ta có: ${{n}_{O{{H}^{-}}}}=1,28 mol>1,08\to $ Al(OH)3 đã bị hòa tan hết
Kết tủa gồm Cu(OH)2 (0,08 mol); Mg(OH)2 (0,1 mol) và BaSO4 (0,16 mol).
$\to {{m}_{kết\ tủa}}=0,08.98+0,1.58+0,16.233=50,92 gam$
Nhận xét: ${{m}_{kết\ tủa\left( TH2 \right)}}<{{m}_{kết\ tủa\left( TH1 \right)}}\to $ Loại TH2.
→ m gam chất rắn khan gồm CuO, MgO, Al2O3 và BaSO4.
Do số mol Cu, Mg, AI được bảo toàn nên ${{m}_{CuO}}+{{m}_{MgO}}+{{m}_{A{{l}_{2}}{{O}_{3}}}}=18,56 gam$
$\to m=18,56+0,115.233=45,355 gam$
Chú ý: Đề bài hỏi tại thời điểm kết tủa thu được là lớn nhất, nếu đem nung két tủa đó thu được bao nhiêu gam chất rắn khan. Tránh nhầm lẫn với:
Trường hợp tìm giá trị lớn nhất của m → Chọn nhầm đáp án D.
Trường hợp tìm khối lượng kết tủa lớn nhất → Chọn nhầm đáp án C.
Đáp án A.