Câu hỏi: Dung dịch X chứa a mol ZnSO4; dung dịch Y chứa b mol AlCl3; dung dịch Z chứa c mol NaOH. Tiến hành 2 thí nghiệm sau:
Thí nghiệm 1: Cho từ từ dung dịch Z vào dung dịch X;
Thí nghiệm 2: Cho từ từ dung dịch Z vào dung dịch Y.
Lượng kết tủa ở 2 thí nghiệm biến đổi theo đồ thị sau đây:
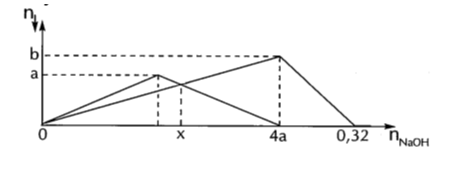
Tổng khối lượng kết tủa ở 2 thí nghiệm khi dùng $x$ mol NaOH gần nhất với giá trị nào sau đây?
A. 9.
B. 8.
C. 8,5.
D. 9,5.
Thí nghiệm 1: Cho từ từ dung dịch Z vào dung dịch X;
Thí nghiệm 2: Cho từ từ dung dịch Z vào dung dịch Y.
Lượng kết tủa ở 2 thí nghiệm biến đổi theo đồ thị sau đây:

Tổng khối lượng kết tủa ở 2 thí nghiệm khi dùng $x$ mol NaOH gần nhất với giá trị nào sau đây?
A. 9.
B. 8.
C. 8,5.
D. 9,5.
Chú ý: đồ thị cho Z vào X có dạng đối xứng, hình tam giác cân (bên trái); đồ thị cho Z vào Y có dạng lệch phải (bên phải).
Xét các điểm đặc biệt trên đồ thị:
Thời điểm 0,32 mol NaOH: là thời điểm NaOH đã phản ứng vừa hết với b mol AlCl3 để chuyển hoàn toàn thành NaAlO2
$\to 4b=0,32\to b=0,08 mol$.
Thời điểm kết tủa Al(OH)3 đạt cực đại, trùng điểm hòa tan vừa hết a mol kết tủa Zn(OH)2
$\to 3b=4\text{a}\to a=0,06 mol$.
Tại thời điểm số mol NaOH bằng x là khi kết tủa Al(OH)3 đang được tạo ra và kết tủa Zn(OH)2 đang bị hòa tan đi. Tại đó số mol của 2 kết tủa bằng nhau:
${{n}_{Al{{\left( OH \right)}_{3}}}}=\dfrac{x}{3}$
$Z{{n}^{2+}}:0,06\xrightarrow{O{{H}^{-}}:x}\left\{ \begin{aligned}
& ZnO_{2}^{2-} \\
& Zn{{\left( OH \right)}_{2}} \\
\end{aligned} \right.$
BT điện tích: $2{{n}_{ZnO_{2}^{2-}}}={{n}_{O{{H}^{-}}}}-2{{n}_{Z{{n}^{2+}}}}\to {{n}_{ZnO_{2}^{2-}}}=\dfrac{{{n}_{O{{H}^{-}}}}-2{{n}_{Z{{n}^{2+}}}}}{2}=\dfrac{x-2\times 0,06}{2}$
BTNT (Zn): ${{n}_{Zn{{\left( OH \right)}_{2}}}}={{n}_{Z{{n}^{2+}}}}-{{n}_{ZnO_{2}^{2-}}}=0,12-0,5\text{x}$
${{n}_{Al{{\left( OH \right)}_{3}}}}={{n}_{Zn{{\left( OH \right)}_{2}}}}\to \dfrac{x}{3}=0,12-0,5\text{x}\to x=0,144$
$\to m=\dfrac{0,144}{3}.\left( 78+99 \right)=8,496$ (gam)
Xét các điểm đặc biệt trên đồ thị:
Thời điểm 0,32 mol NaOH: là thời điểm NaOH đã phản ứng vừa hết với b mol AlCl3 để chuyển hoàn toàn thành NaAlO2
$\to 4b=0,32\to b=0,08 mol$.
Thời điểm kết tủa Al(OH)3 đạt cực đại, trùng điểm hòa tan vừa hết a mol kết tủa Zn(OH)2
$\to 3b=4\text{a}\to a=0,06 mol$.
Tại thời điểm số mol NaOH bằng x là khi kết tủa Al(OH)3 đang được tạo ra và kết tủa Zn(OH)2 đang bị hòa tan đi. Tại đó số mol của 2 kết tủa bằng nhau:
${{n}_{Al{{\left( OH \right)}_{3}}}}=\dfrac{x}{3}$
$Z{{n}^{2+}}:0,06\xrightarrow{O{{H}^{-}}:x}\left\{ \begin{aligned}
& ZnO_{2}^{2-} \\
& Zn{{\left( OH \right)}_{2}} \\
\end{aligned} \right.$
BT điện tích: $2{{n}_{ZnO_{2}^{2-}}}={{n}_{O{{H}^{-}}}}-2{{n}_{Z{{n}^{2+}}}}\to {{n}_{ZnO_{2}^{2-}}}=\dfrac{{{n}_{O{{H}^{-}}}}-2{{n}_{Z{{n}^{2+}}}}}{2}=\dfrac{x-2\times 0,06}{2}$
BTNT (Zn): ${{n}_{Zn{{\left( OH \right)}_{2}}}}={{n}_{Z{{n}^{2+}}}}-{{n}_{ZnO_{2}^{2-}}}=0,12-0,5\text{x}$
${{n}_{Al{{\left( OH \right)}_{3}}}}={{n}_{Zn{{\left( OH \right)}_{2}}}}\to \dfrac{x}{3}=0,12-0,5\text{x}\to x=0,144$
$\to m=\dfrac{0,144}{3}.\left( 78+99 \right)=8,496$ (gam)
Đáp án C.