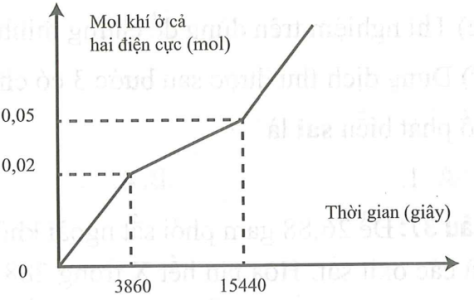
Câu hỏi: Điện phân dung dịch X chứa $Cu{{\left( N{{O}_{3}} \right)}_{2}}$ và $KCl$ với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi $I=1A$. Số mol khí sinh ra ở cả hai điện cực (mol) theo thời gian điện phân t (giây) được biểu diễn như hình vẽ, hiệu suất điện phân 100%, các khí sinh ra không tan trong nước.
Nếu điện phân dung dịch X trong thời gian 11580 giây rồi cho dung dịch sau điện phân tác dụng với lượng dư Mg thấy có 0,01 mol NO thoát ra. Dung dịch sau phản ứng chứa m gam chất tan. Giá trị của m là
A. 11,908
B. 11,836
C. 12,106
D. 11,424

Nếu điện phân dung dịch X trong thời gian 11580 giây rồi cho dung dịch sau điện phân tác dụng với lượng dư Mg thấy có 0,01 mol NO thoát ra. Dung dịch sau phản ứng chứa m gam chất tan. Giá trị của m là
A. 11,908
B. 11,836
C. 12,106
D. 11,424
Giai đoạn 1: Khí $C{{l}_{2}}$ thoát ra. $C{{l}^{-}}$ điện phân hết.
${{n}_{C{{l}_{2}}}}=0,02\to {{n}_{KCl}}=0,04$
Giai đoạn 2: Khí ${{O}_{2}}$ thoát ra.
$t=15440\to {{n}_{e}}=0,16$
Lúc này chỉ có khí ${{O}_{2}}$ và $C{{l}_{2}}$, khí ${{H}_{2}}$ sẽ bắt đầu xuất hiện ở giai đoạn sau, nên $C{{u}^{2+}}$ điện phân hết.
$\to {{n}_{C{{u}^{2+}} \text{ban u}}}=\dfrac{1}{2}{{n}_{e}}=0,08$
$t=15440\to {{n}_{e}}=0,12$
$\begin{aligned}
& C{{u}^{2+}}+2e\to Cu 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& 0,06 \leftarrow 0,12 0,02 0,04 \\
& 2{{H}_{2}}O\to 4{{H}^{+}}+{{O}_{2}}+4e \\
\end{aligned}$
BT e: ${{n}_{{{H}^{+}}}}=0,12-0,04=0,08$
Vậy dung dịch sau điện phân chứa:
$\left\{ \begin{aligned}
& C{{u}^{2+}}:0,08-0,06=0,02 \\
& {{H}^{+}}:0,08 \\
& NO_{3}^{-}:0,16(BT\S T) \\
& {{K}^{+}}:0,04\left( {{n}_{KCl}} \right) \\
\end{aligned} \right.$
$\begin{aligned}
& Mg\xrightarrow{{}}M{{g}^{2+}}+2e 4{{H}^{+}}+NO_{3}^{-}+3e\xrightarrow{{}}NO+2{{H}_{2}}O \\
& 0,04 0,01 0,03 \leftarrow 0,01 \\
& 10{{H}^{+}}+NO_{3}^{-}+8e\xrightarrow{{}}NH_{4}^{+}+3{{H}_{2}}O \\
& 0,04 0,15 \\
& 0,04 0,004 0,032 0,004 \\
& C{{u}^{2+}}+2e\xrightarrow{{}}Cu \\
& 0,02\to 0,04 \\
\end{aligned}$
$\left\{ \begin{aligned}
& M{{g}^{2+}}:0,051 \left( BT \S T \right) \\
& NH_{4}^{+}:0,004 \\
& NO_{3}^{-}:0,146 \\
& {{K}^{+}}:0,04 \left( {{n}_{KCl}} \right) \\
\end{aligned} \right.\to m=11,908$
${{n}_{C{{l}_{2}}}}=0,02\to {{n}_{KCl}}=0,04$
Giai đoạn 2: Khí ${{O}_{2}}$ thoát ra.
$t=15440\to {{n}_{e}}=0,16$
Lúc này chỉ có khí ${{O}_{2}}$ và $C{{l}_{2}}$, khí ${{H}_{2}}$ sẽ bắt đầu xuất hiện ở giai đoạn sau, nên $C{{u}^{2+}}$ điện phân hết.
$\to {{n}_{C{{u}^{2+}} \text{ban u}}}=\dfrac{1}{2}{{n}_{e}}=0,08$
$t=15440\to {{n}_{e}}=0,12$
$\begin{aligned}
& C{{u}^{2+}}+2e\to Cu 2C{{l}^{-}}\to C{{l}_{2}}+2e \\
& 0,06 \leftarrow 0,12 0,02 0,04 \\
& 2{{H}_{2}}O\to 4{{H}^{+}}+{{O}_{2}}+4e \\
\end{aligned}$
BT e: ${{n}_{{{H}^{+}}}}=0,12-0,04=0,08$
Vậy dung dịch sau điện phân chứa:
$\left\{ \begin{aligned}
& C{{u}^{2+}}:0,08-0,06=0,02 \\
& {{H}^{+}}:0,08 \\
& NO_{3}^{-}:0,16(BT\S T) \\
& {{K}^{+}}:0,04\left( {{n}_{KCl}} \right) \\
\end{aligned} \right.$
$\begin{aligned}
& Mg\xrightarrow{{}}M{{g}^{2+}}+2e 4{{H}^{+}}+NO_{3}^{-}+3e\xrightarrow{{}}NO+2{{H}_{2}}O \\
& 0,04 0,01 0,03 \leftarrow 0,01 \\
& 10{{H}^{+}}+NO_{3}^{-}+8e\xrightarrow{{}}NH_{4}^{+}+3{{H}_{2}}O \\
& 0,04 0,15 \\
& 0,04 0,004 0,032 0,004 \\
& C{{u}^{2+}}+2e\xrightarrow{{}}Cu \\
& 0,02\to 0,04 \\
\end{aligned}$
$\left\{ \begin{aligned}
& M{{g}^{2+}}:0,051 \left( BT \S T \right) \\
& NH_{4}^{+}:0,004 \\
& NO_{3}^{-}:0,146 \\
& {{K}^{+}}:0,04 \left( {{n}_{KCl}} \right) \\
\end{aligned} \right.\to m=11,908$
Đáp án A.