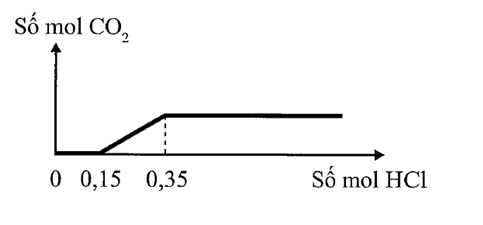
Câu hỏi: Cho từ từ dung dịch HCl vào dung dịch có chứa a mol NaHCO3 và b mol Na2CO3. Số mol khí CO2 thu được phụ thuộc vào số mol HCl được biểu diễn trên đồ thị sau: Tỉ lệ của a : b bằng
A. 1 : 3.
B. 3 : 4.
C. 7 : 3.
D. 4 : 3.

A. 1 : 3.
B. 3 : 4.
C. 7 : 3.
D. 4 : 3.
${{n}_{HCO_{3}^{-}}}=a mol;{{n}_{CO_{3}^{2-}}}=b mol$
Cho từ từ dung dịch HCl vào dung dịch chứa NaHCO3 và Na2CO3 ta có thứ tự phản ứng:
$CO_{3}^{2-}+{{H}^{+}}\to HCO_{3}^{-}$ (1)
$HCO_{3}^{-}+{{H}^{-}}\to C{{O}_{2}}+{{H}_{2}}O$ (2)
Từ ${{n}_{HCl}}=0 mol\to {{n}_{HCl}}=0,15 mol$, xảy ra phương trình (1):
${{n}_{CO_{3}^{2-}}}={{n}_{{{H}^{+}}}}={{n}_{HCl\left( 1 \right)}}=0,15 mol$
$\to b=0,15$
Từ ${{n}_{HCl}}=0,15 mol\to {{n}_{HCl}}=0,35 mol$, xảy ra phương trình (2): ${{n}_{C{{O}_{2}}}}={{n}_{HCl\left( 2 \right)}}=0,35-0,15=0,2 mol$
Bảo toàn nguyên tố C: ${{n}_{HCO_{3}^{-}}}+{{n}_{CO_{3}^{-}}}={{n}_{C{{O}_{2}}}}=0,2 mol$
$\to {{n}_{HCO_{3}^{-}}}=0,2-0,15=0,05 mol$
$\to a=0,05$
$\to a:b=0,05:0,15=1:3$
Cho từ từ dung dịch HCl vào dung dịch chứa NaHCO3 và Na2CO3 ta có thứ tự phản ứng:
$CO_{3}^{2-}+{{H}^{+}}\to HCO_{3}^{-}$ (1)
$HCO_{3}^{-}+{{H}^{-}}\to C{{O}_{2}}+{{H}_{2}}O$ (2)
Từ ${{n}_{HCl}}=0 mol\to {{n}_{HCl}}=0,15 mol$, xảy ra phương trình (1):
${{n}_{CO_{3}^{2-}}}={{n}_{{{H}^{+}}}}={{n}_{HCl\left( 1 \right)}}=0,15 mol$
$\to b=0,15$
Từ ${{n}_{HCl}}=0,15 mol\to {{n}_{HCl}}=0,35 mol$, xảy ra phương trình (2): ${{n}_{C{{O}_{2}}}}={{n}_{HCl\left( 2 \right)}}=0,35-0,15=0,2 mol$
Bảo toàn nguyên tố C: ${{n}_{HCO_{3}^{-}}}+{{n}_{CO_{3}^{-}}}={{n}_{C{{O}_{2}}}}=0,2 mol$
$\to {{n}_{HCO_{3}^{-}}}=0,2-0,15=0,05 mol$
$\to a=0,05$
$\to a:b=0,05:0,15=1:3$
Đáp án A.