Câu hỏi: Cho m gam hỗn hợp gồm Na2O và Al2O3 vào 400 ml dung dịch H2SO4 0,3M và HCl 0,9M. Sau khi kết thúc phản ứng, thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X, phản ứng được biểu diễn theo đồ thị sau:
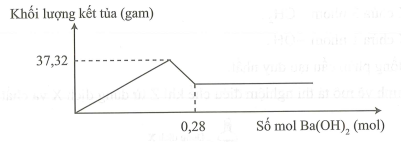
Giá trị của m là?
A. 16,04 gam
B. 17,2 gam
C. 11,08 gam
D. 9,84 gam

Giá trị của m là?
A. 16,04 gam
B. 17,2 gam
C. 11,08 gam
D. 9,84 gam
${{m}_{\downarrow \max }}={{m}_{BaS{{O}_{4}}}}+{{m}_{Al{{\left( OH \right)}_{3}}}}\to 233.{{n}_{SO_{4}^{2-}}}+78.{{n}_{Al{{\left( OH \right)}_{3}}}}=37,32$
$\to 233.0,12+78.{{n}_{Al{{\left( OH \right)}_{3}}}}=37,32\to {{n}_{Al{{\left( OH \right)}_{3}}}}=0,12$
Khi kết tủa không đổi là lúc kết tủa Al(OH)3 tan hết
$A{{l}^{3+}}+3O{{H}^{-}}\to Al{{\left( OH \right)}_{3}}$
0,120,36
$Al{{\left( OH \right)}_{3}}+O{{H}^{-}}\to AlO_{2}^{-}+2{{H}_{2}}O$
0,12 0,12
Lúc này ${{n}_{O{{H}^{-}}}}=0,36+0,12=0,48$
Theo đồ thị ${{n}_{Ba{{\left( OH \right)}_{2}}}}=0,28\to {{n}_{O{{H}^{-}}}}=0,56$
Chứng tỏ trong dung dịch X có axit:
${{H}^{+}}+O{{H}^{-}}\to {{H}_{2}}O$
$\to {{n}_{{{H}^{+}}}}=0,56-0,48=0,08$
Vậy trong X chứa: $\left\{ \begin{aligned}
& C{{l}^{-}}:0,36 \\
& SO_{4}^{2-}:0,12 \\
& {{H}^{+}}:0,08 \\
& A{{l}^{3+}}:0,12\left( BTAl \right) \\
& N{{a}^{+}}:0,16\left( BTDT \right) \\
\end{aligned} \right.\to m\left\{ \begin{aligned}
& N{{a}_{2}}O:0,08 \\
& A{{l}_{2}}{{O}_{3}}:0,06 \\
\end{aligned} \right.\to m=11,08$gam.
$\to 233.0,12+78.{{n}_{Al{{\left( OH \right)}_{3}}}}=37,32\to {{n}_{Al{{\left( OH \right)}_{3}}}}=0,12$
Khi kết tủa không đổi là lúc kết tủa Al(OH)3 tan hết
$A{{l}^{3+}}+3O{{H}^{-}}\to Al{{\left( OH \right)}_{3}}$
0,120,36
$Al{{\left( OH \right)}_{3}}+O{{H}^{-}}\to AlO_{2}^{-}+2{{H}_{2}}O$
0,12 0,12
Lúc này ${{n}_{O{{H}^{-}}}}=0,36+0,12=0,48$
Theo đồ thị ${{n}_{Ba{{\left( OH \right)}_{2}}}}=0,28\to {{n}_{O{{H}^{-}}}}=0,56$
Chứng tỏ trong dung dịch X có axit:
${{H}^{+}}+O{{H}^{-}}\to {{H}_{2}}O$
$\to {{n}_{{{H}^{+}}}}=0,56-0,48=0,08$
Vậy trong X chứa: $\left\{ \begin{aligned}
& C{{l}^{-}}:0,36 \\
& SO_{4}^{2-}:0,12 \\
& {{H}^{+}}:0,08 \\
& A{{l}^{3+}}:0,12\left( BTAl \right) \\
& N{{a}^{+}}:0,16\left( BTDT \right) \\
\end{aligned} \right.\to m\left\{ \begin{aligned}
& N{{a}_{2}}O:0,08 \\
& A{{l}_{2}}{{O}_{3}}:0,06 \\
\end{aligned} \right.\to m=11,08$gam.
Đáp án C.