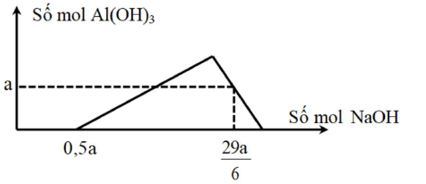
Câu hỏi: Cho m gam Al tác dụng với ${{O}_{2}}$, sau một thời gian thu được (m + 2,88) gam hỗn hợp X. Cho hỗn hợp X tác dụng với dung dịch HCl dư, thu được a mol ${{H}_{2}}$ và dung dịch Y. Rót từ từ dung dịch NaOH vào dung dịch Y ta có đồ thị sau:
có đồ thị sau:
Cho hỗn hợp X tác dụng với dung dịch $HN{{O}_{3}}$ dư, thu được V lít hỗn hợp khí NO và ${{N}_{2}}O$ (đktc) có tỉ khối so với hidro là 16,75 và dung dịch Z. Cô cạn dung dịch X thu được $\left( m+\dfrac{2242}{9}a \right)$ gam chất rắn khan. Giá trị của V gần nhất với giá trị nào dưới đây?
A. 1,8.
B. 2,1.
C. 2,3.
D. 1,7
có đồ thị sau:

Cho hỗn hợp X tác dụng với dung dịch $HN{{O}_{3}}$ dư, thu được V lít hỗn hợp khí NO và ${{N}_{2}}O$ (đktc) có tỉ khối so với hidro là 16,75 và dung dịch Z. Cô cạn dung dịch X thu được $\left( m+\dfrac{2242}{9}a \right)$ gam chất rắn khan. Giá trị của V gần nhất với giá trị nào dưới đây?
A. 1,8.
B. 2,1.
C. 2,3.
D. 1,7
Phương pháp:
- Quy đổi hỗn hợp X thành Al và O
- Phương pháp đường chéo
- Công thức tính nhanh bài toán cho từ từ $O{{H}^{-}}$ vào ${{H}^{+}};A{{l}^{3+}}$
Thứ tự phản ứng khi cho từ từ $O{{H}^{-}}$ vào ${{H}^{+}};A{{l}^{3+}}$ là:
$\left( 1 \right)O{{H}^{-}}+{{H}^{+}}\to {{H}_{2}}O$
$\left( 2 \right)A{{1}^{3+}}+3O{{H}^{-}}\to Al{{\left( OH \right)}_{3}}~$
$\left( 3 \right)Al{{\left( OH \right)}_{3}}+O{{H}^{-}}\to A1{{O}_{2}}^{-}+2{{H}_{2}}O$
Như vậy, khi cho từ từ $O{{H}^{-}}$ vào ${{H}^{+}};A{{l}^{3+}}$ thì:
- Đầu tiên, $O{{H}^{-}}$ trung hòa ${{H}^{+}}$ nên chưa thấy xuất hiện kết tủa, khi đó chỉ xảy ra (1)
$\to {{n}_{OH-}}_{\left( 1 \right)}={{n}_{H+}}$
- Khi ${{H}^{+}}$ bị trung hòa hết, kết tủa sẽ tăng từ từ cho đến khi cực đại khi đó xảy ra (2)
$\to {{\text{n}}_{OH-\left( 2 \right)}}=3{{n}_{A13+}}$
- Khi NaOH dư thì kết tủa sẽ bị tan dần cho đến hết khi đó xảy ra (3)
$\to {{n}_{OH-\left( 3 \right)}}={{n}_{Al\left( OH \right)3bi \tan }}={{n}_{Al3+}}-{{n}_{Al{{\left( OH \right)}_{3}}}}$
Vậy ta có công thức tính nhanh của trường hợp kết tủa tan:
$\sum{{{n}_{OH-}}}={{n}_{H+}}+3{{n}_{Al3+}}+{{n}_{Al3+}}-{{\text{n}}_{Al\left( OH \right)3}}={{n}_{H+}}+4{{n}_{Al3+}}-{{n}_{Al\left( OH \right)3}}$
Hướng dẫn giải:
Quy đổi hỗn hợp X thành Al và O
${{m}_{O}}={{m}_{X}}-{{m}_{Al}}=2,88gam\to {{n}_{O}}=\text{ =}0,18mol$
- Khi cho X tác dụng với HCl dư, bảo toàn e $\to 3{{n}_{Al}}=2{{n}_{O}}+2{{n}_{H2}}~$
$\to 3{{n}_{Al}}=2.0,18+2a\to {{n}_{Al}}=\left( 2a+0,36 \right)/3~$
Dung dịch Y chứa: $A{{l}^{3+}}\left( \dfrac{2a+0,36}{3} \right):{{H}^{+}}~v\grave{a}C{{l}^{-}}~$
- Cho từ từ $O{{H}^{-}}$ vào Y:
+ Khi ${{n}_{OH-}}=0,5a$ mol thì ${{H}^{+}}$ vừa bị trung hòa hết
$\to {{n}_{H+}}={{n}_{OH-}}=0,5a\left( mol \right)$
+ Khi ${{n}_{OH-}}=29a/6mol$ thì $Al{{\left( OH \right)}_{3}}$ bị hòa tan một phần.
Ta có công thức tính nhanh (xem chứng minh ở phần phương pháp):
${{n}_{OH-}}={{n}_{H+}}+4{{n}_{Al3+}}-{{n}_{Al\left( OH \right)3}}~$
$\to \dfrac{29a}{6}=0,5a+4.\dfrac{2a+0,36}{3}~~-a~\to a=0,18~$
Vậy X chứa A1 (0,24) và O (0,18)
- Cho X tác dụng với HNO3 dư:
$m=0,24.27=6,48gamv\grave{a}{{m}_{muoi}}=m+\dfrac{2242}{9}a=51,32gam~$
Ta thấy: $m{{A}_{l\left( NO3 \right)3}}=0,24.213=51,12gam<{{m}_{muoi}}~$
$\to $ Muối có ${{n}_{N{{H}_{4}}N{{O}_{3}}}}=(51,32-51,12)/80=0,0025mol$
${{M}_{kh\acute{i}}}=16,75.2=33,5$
Áp dụng phương pháp đường chéo:
$\begin{aligned}
& NO: 30 10,5 \\
& \text{33}\text{,5 } \\
& {{N}_{2}}O:44~ 3,5 \\
\end{aligned}$
$\to {{n}_{NO}}:{{n}_{N2O}}=3:1$
Giả sử ${{n}_{NO}}=3xv\grave{a}{{n}_{N2O}}=x\left( mol \right)$
Áp dụng bảo toàn e: $3{{n}_{Al}}=2{{n}_{O}}+3{{n}_{NO}}+8{{n}_{N2O}}+8{{n}_{NH4NO3}}~$
$\to 3.0,24=2.0,18+3.3x+8x+8.0,0025\to x=0,02$
$\to V=22,4\left( 3x+x \right)=1,792$ lít gần nhất với 1,8 lít
- Quy đổi hỗn hợp X thành Al và O
- Phương pháp đường chéo
- Công thức tính nhanh bài toán cho từ từ $O{{H}^{-}}$ vào ${{H}^{+}};A{{l}^{3+}}$
Thứ tự phản ứng khi cho từ từ $O{{H}^{-}}$ vào ${{H}^{+}};A{{l}^{3+}}$ là:
$\left( 1 \right)O{{H}^{-}}+{{H}^{+}}\to {{H}_{2}}O$
$\left( 2 \right)A{{1}^{3+}}+3O{{H}^{-}}\to Al{{\left( OH \right)}_{3}}~$
$\left( 3 \right)Al{{\left( OH \right)}_{3}}+O{{H}^{-}}\to A1{{O}_{2}}^{-}+2{{H}_{2}}O$
Như vậy, khi cho từ từ $O{{H}^{-}}$ vào ${{H}^{+}};A{{l}^{3+}}$ thì:
- Đầu tiên, $O{{H}^{-}}$ trung hòa ${{H}^{+}}$ nên chưa thấy xuất hiện kết tủa, khi đó chỉ xảy ra (1)
$\to {{n}_{OH-}}_{\left( 1 \right)}={{n}_{H+}}$
- Khi ${{H}^{+}}$ bị trung hòa hết, kết tủa sẽ tăng từ từ cho đến khi cực đại khi đó xảy ra (2)
$\to {{\text{n}}_{OH-\left( 2 \right)}}=3{{n}_{A13+}}$
- Khi NaOH dư thì kết tủa sẽ bị tan dần cho đến hết khi đó xảy ra (3)
$\to {{n}_{OH-\left( 3 \right)}}={{n}_{Al\left( OH \right)3bi \tan }}={{n}_{Al3+}}-{{n}_{Al{{\left( OH \right)}_{3}}}}$
Vậy ta có công thức tính nhanh của trường hợp kết tủa tan:
$\sum{{{n}_{OH-}}}={{n}_{H+}}+3{{n}_{Al3+}}+{{n}_{Al3+}}-{{\text{n}}_{Al\left( OH \right)3}}={{n}_{H+}}+4{{n}_{Al3+}}-{{n}_{Al\left( OH \right)3}}$
Hướng dẫn giải:
Quy đổi hỗn hợp X thành Al và O
${{m}_{O}}={{m}_{X}}-{{m}_{Al}}=2,88gam\to {{n}_{O}}=\text{ =}0,18mol$
- Khi cho X tác dụng với HCl dư, bảo toàn e $\to 3{{n}_{Al}}=2{{n}_{O}}+2{{n}_{H2}}~$
$\to 3{{n}_{Al}}=2.0,18+2a\to {{n}_{Al}}=\left( 2a+0,36 \right)/3~$
Dung dịch Y chứa: $A{{l}^{3+}}\left( \dfrac{2a+0,36}{3} \right):{{H}^{+}}~v\grave{a}C{{l}^{-}}~$
- Cho từ từ $O{{H}^{-}}$ vào Y:
+ Khi ${{n}_{OH-}}=0,5a$ mol thì ${{H}^{+}}$ vừa bị trung hòa hết
$\to {{n}_{H+}}={{n}_{OH-}}=0,5a\left( mol \right)$
+ Khi ${{n}_{OH-}}=29a/6mol$ thì $Al{{\left( OH \right)}_{3}}$ bị hòa tan một phần.
Ta có công thức tính nhanh (xem chứng minh ở phần phương pháp):
${{n}_{OH-}}={{n}_{H+}}+4{{n}_{Al3+}}-{{n}_{Al\left( OH \right)3}}~$
$\to \dfrac{29a}{6}=0,5a+4.\dfrac{2a+0,36}{3}~~-a~\to a=0,18~$
Vậy X chứa A1 (0,24) và O (0,18)
- Cho X tác dụng với HNO3 dư:
$m=0,24.27=6,48gamv\grave{a}{{m}_{muoi}}=m+\dfrac{2242}{9}a=51,32gam~$
Ta thấy: $m{{A}_{l\left( NO3 \right)3}}=0,24.213=51,12gam<{{m}_{muoi}}~$
$\to $ Muối có ${{n}_{N{{H}_{4}}N{{O}_{3}}}}=(51,32-51,12)/80=0,0025mol$
${{M}_{kh\acute{i}}}=16,75.2=33,5$
Áp dụng phương pháp đường chéo:
$\begin{aligned}
& NO: 30 10,5 \\
& \text{33}\text{,5 } \\
& {{N}_{2}}O:44~ 3,5 \\
\end{aligned}$
$\to {{n}_{NO}}:{{n}_{N2O}}=3:1$
Giả sử ${{n}_{NO}}=3xv\grave{a}{{n}_{N2O}}=x\left( mol \right)$
Áp dụng bảo toàn e: $3{{n}_{Al}}=2{{n}_{O}}+3{{n}_{NO}}+8{{n}_{N2O}}+8{{n}_{NH4NO3}}~$
$\to 3.0,24=2.0,18+3.3x+8x+8.0,0025\to x=0,02$
$\to V=22,4\left( 3x+x \right)=1,792$ lít gần nhất với 1,8 lít
Đáp án A.