Câu hỏi: Cho $ 3,1 $ gam hỗn hợp hai kim loại kiềm ở hai chu kì liên tiếp trong bảng tuần hoàn tác dụng hết với nước thu được dung dịch kiềm và $ 1,12 $ lít $ {H_2} $ (đktc).
a) Xác định tên kim loại kiềm và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp
b) Tính thể tích dung dịch $ HCl 2M $ cần dùng để trung hòa dung dịch kiềm trên và khối lượng hỗn hợp muối clorua thu được.
a) Xác định tên kim loại kiềm và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp
b) Tính thể tích dung dịch $ HCl 2M $ cần dùng để trung hòa dung dịch kiềm trên và khối lượng hỗn hợp muối clorua thu được.
a) Đặt ký hiệu của kim loại kiềm thứ 1 là A, khối lượng mol là A ( mol); kim loại kiềm thứ 2 là B, khối lượng mol là B (y mol).
Ký hiệu chung M là khối lượng mol nguyên tử trung bình của hai kim loại
Ta có: $ {n_{{H_2}}} $ $ = {{1,12} \over {22,4}} = 0,05\left(mol\right) $
$ 2M + 2{H_2}O \Rightarrow 2MOH + {H_2}. $
$ 0,1 $ $ \leftarrow $ $ 0,05 $
$ M = {{3,1} \over {0,1}} = 31 \Rightarrow A = 23 \left(Na\right) = 23 < M = 31 < B = 39 \left(K\right) $
Vậy hai kim loại kiềm đó là: $ Na $ và $ K $.
Cách 1:
Ta có:
$ \left\{ \matrix{
x + y = 0,1 \hfill \cr
23x + 39y = 3,1 \hfill \cr} \right. \Rightarrow \left\{ \matrix{
x = 0,05 \hfill \cr
y = 0,05 \hfill \cr} \right. \Rightarrow \left\{ \matrix{
{m_{Na}} = 0,05.23 = 1,15\left(g\right) \hfill \cr
{m_K} = 0,05.39 = 1,95\left(g\right) \hfill \cr} \right. $
Thành phần phần trăm khối lượng:
$ \eqalign{
& \% {m_{Na}} = {{1,15} \over {3,1}}.100 = 37,1\% \cr
& \% {m_K} = {{1,95} \over {3,1}}.100 = 62,9\% \cr} $
b) Phương trình phản ứng
$ \eqalign{
& NaOH + HCl \Rightarrow NaCl + {H_2}0. \cr
& 0,05 \Rightarrow 0,05 \Rightarrow 0,05 \cr
&KOH + HCl \Rightarrow KCl + {H_2}O \cr
& 0,05 \Rightarrow 0,05 \Rightarrow 0,05 \cr
& \Rightarrow {n_{HCl}} = 0,05 + 0,05 = 0,1 \Rightarrow {V_{HCl}} = {{0,1} \over 2} = 0,05\left(l\right) = 50 \left(ml\right) \cr
& \Rightarrow {m_{Muối}} = 0,05.58,5 + 0,05.74,5 = 6,65\left(g\right). \cr
& \cr} $
Cách 2:
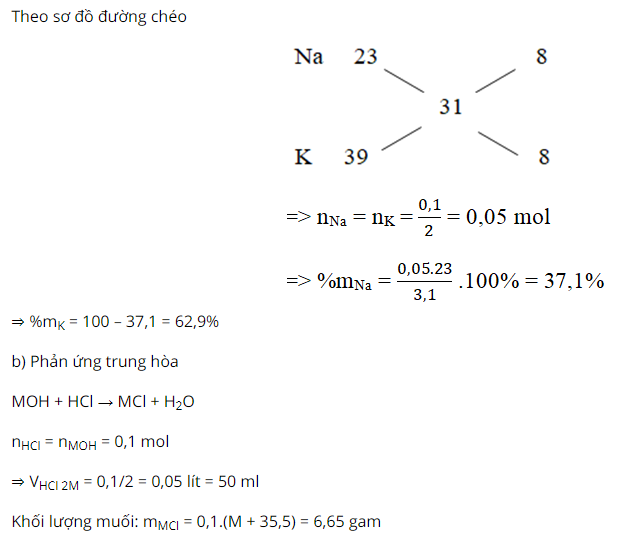
Ký hiệu chung M là khối lượng mol nguyên tử trung bình của hai kim loại
Ta có: $ {n_{{H_2}}} $ $ = {{1,12} \over {22,4}} = 0,05\left(mol\right) $
$ 2M + 2{H_2}O \Rightarrow 2MOH + {H_2}. $
$ 0,1 $ $ \leftarrow $ $ 0,05 $
$ M = {{3,1} \over {0,1}} = 31 \Rightarrow A = 23 \left(Na\right) = 23 < M = 31 < B = 39 \left(K\right) $
Vậy hai kim loại kiềm đó là: $ Na $ và $ K $.
Cách 1:
Ta có:
$ \left\{ \matrix{
x + y = 0,1 \hfill \cr
23x + 39y = 3,1 \hfill \cr} \right. \Rightarrow \left\{ \matrix{
x = 0,05 \hfill \cr
y = 0,05 \hfill \cr} \right. \Rightarrow \left\{ \matrix{
{m_{Na}} = 0,05.23 = 1,15\left(g\right) \hfill \cr
{m_K} = 0,05.39 = 1,95\left(g\right) \hfill \cr} \right. $
Thành phần phần trăm khối lượng:
$ \eqalign{
& \% {m_{Na}} = {{1,15} \over {3,1}}.100 = 37,1\% \cr
& \% {m_K} = {{1,95} \over {3,1}}.100 = 62,9\% \cr} $
b) Phương trình phản ứng
$ \eqalign{
& NaOH + HCl \Rightarrow NaCl + {H_2}0. \cr
& 0,05 \Rightarrow 0,05 \Rightarrow 0,05 \cr
&KOH + HCl \Rightarrow KCl + {H_2}O \cr
& 0,05 \Rightarrow 0,05 \Rightarrow 0,05 \cr
& \Rightarrow {n_{HCl}} = 0,05 + 0,05 = 0,1 \Rightarrow {V_{HCl}} = {{0,1} \over 2} = 0,05\left(l\right) = 50 \left(ml\right) \cr
& \Rightarrow {m_{Muối}} = 0,05.58,5 + 0,05.74,5 = 6,65\left(g\right). \cr
& \cr} $
Cách 2: