Câu hỏi: Hòa tan hoàn toàn m gam hỗn hợp X gồm Al và Mg trong 500ml dung dịch HNO3 1M thu được dung dịch Y và khí NO (sản phẩm khử duy nhất). Cho từ từ dung dịch NaOH vào dung dịch Y, lượng kết tủa tạo thành được biểu diễn theo đồ thị sau:
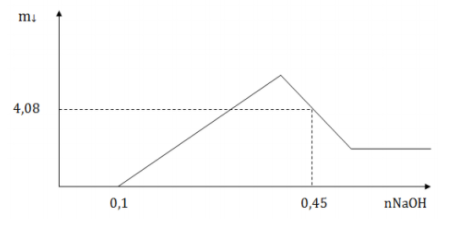
Giá trị của m là
A. 3,24
B. 3,06
C. 2,79
D. 2,88

Giá trị của m là
A. 3,24
B. 3,06
C. 2,79
D. 2,88
Khi ${{n}_{O{{H}^{-}}}}=0,1$ thì kết tủa mới xuất hiện nên ${{n}_{{{H}^{+}}}}$ dư = 0,1
$\to {{n}_{{{H}^{+}}}}$ phản ứng = 0,4
$\to {{n}_{NO}}=0,1$
Đặt a, b là số mol Al và Mg
$\to 3a+2b=0,1.3\left( 1 \right)$
Khi ${{n}_{O{{H}^{-}}}}=0,45$ thì kết tủa gồm Mg(OH)2 (b) và $Al{{\left( OH \right)}_{3}}\frac{4,08-58b}{78}$
$\to 0,45=0,1+2b+4a-\frac{4,08-58b}{78}\left( 2 \right)$
$\left( 1 \right)\left( 2 \right)\to a=0,08$ và $b=0,03$
$\to m=2,88$
$\to {{n}_{{{H}^{+}}}}$ phản ứng = 0,4
$\to {{n}_{NO}}=0,1$
Đặt a, b là số mol Al và Mg
$\to 3a+2b=0,1.3\left( 1 \right)$
Khi ${{n}_{O{{H}^{-}}}}=0,45$ thì kết tủa gồm Mg(OH)2 (b) và $Al{{\left( OH \right)}_{3}}\frac{4,08-58b}{78}$
$\to 0,45=0,1+2b+4a-\frac{4,08-58b}{78}\left( 2 \right)$
$\left( 1 \right)\left( 2 \right)\to a=0,08$ và $b=0,03$
$\to m=2,88$
Đáp án D.