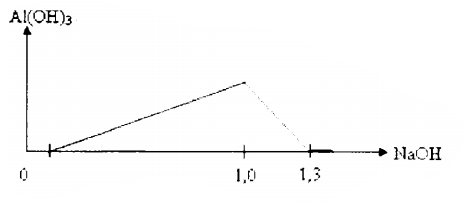
Câu hỏi: Hòa tan 10,92 gam hỗn hợp X chứa Al, Al2O3 và Al(NO3)3 vào dung dịch chứa NaHSO4 và 0,09 mol HNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chứa các chất tan có khối lượng 127,88 gam và 0,08 mol hỗn hợp khí Z gồm 3 khí không màu, không hóa nâu ngoài không khí. Tỉ khối hơi của Z so với He bằng 5. Cho từ từ đến dư dung dịch NaOH vào dung dịch Y, phản ứng được biểu diễn theo đồ thị sau:
Phần trăm khối lượng của khí có khối lượng phân tử lớn nhất trong hỗn hợp Z là
A. 41,25%.
B. 68,75%
C. 55,00%.
D. 82,50%.
Phần trăm khối lượng của khí có khối lượng phân tử lớn nhất trong hỗn hợp Z là
A. 41,25%.
B. 68,75%
C. 55,00%.
D. 82,50%.
Giả thiết $\Rightarrow $ Z gồm N2O, N2, H2 $\Rightarrow $ Y không chứa $N{{O}_{3}}^{-}$ ;khí có M lớn nhất trong Z là N2O
$\underbrace{\left\{ \begin{matrix}
Al \\
A{{l}_{2}}{{O}_{3}} \\
Al{{(N{{O}_{3}})}_{3}} \\
\end{matrix} \right\}}_{10,92(g)}+\left\{ \begin{matrix}
NaHS{{O}_{4}} \\
HN{{O}_{3}}:0,09 \\
\end{matrix} \right\}\to \left\{ \begin{matrix}
{{N}_{2}}O \\
{{N}_{2}} \\
{{H}_{2}} \\
\end{matrix} \right\}+{{H}_{2}}O+\left\{ \begin{matrix}
A{{l}^{3+}} \\
N{{a}^{+}} \\
NH_{4}^{+} \\
{{H}^{+}} \\
SO_{4}^{2-} \\
\end{matrix} \right\}$
Từ 1 mol NaOH đến 1,3 mol NaOH thì kết tủa từ cực đại đến tan hết do xảy ra phản ứng:
$Al{{(OH)}_{3}}+NaOH\to NaA1{{O}_{2}}+2{{H}_{2}}O\to {{n}_{A{{l}^{3+}}}}={{n}_{Al{{(OH)}_{3}}}}=1,3-1=0,3mol.$
Đặt ${{n}_{NaHS{{0}_{4}}}}=x\ mol\to {{n}_{N{{a}^{+}}/Y}}={{n}_{SO_{4}^{2-}}}=x\ mol.$
Khi kết tủa đạt cực đại thì chỉ thu được Na2SO4.
$\to {{n}_{N{{a}_{2}}S{{0}_{4}}}}=x\ mol\Rightarrow \sum{{{n}_{N{{a}^{+}}}}}=2x\to {{n}_{N{{a}^{+}}/Y}}=2x-1=x\Rightarrow x=1.$
Đặt ${{n}_{NH_{4}^{+}}}$ = y mol; ${{n}_{{{H}^{+}}}}$ = z mol. Bảo toàn điện tích: 0,3.3 +l + y+z=1.2
mmuối = 127,88(g) = 0,3 . 27 + 1 . 23 + 18y + z + 1 . 96
Giải hệ có: y = 0,04 mol; z = 0,06 mol. Bảo toàn khối lượng:
${{m}_{H20}}$ = 10,92 + 1 . 120 + 0,09 .63 - 127,88 - 0,08 .20 = 7,1 lg $\Rightarrow {{n}_{{{H}_{2}}O}}$ = 0,395 mol.
Bảo toàn nguyên tố hiđro: ${{n}_{{{H}_{2}}}}$ = (1 + 0,09 - 0,04 .4 - 0,06 - 0,395.2)/2 - 0,04 mol.
Đặt ${{n}_{{{N}_{2}}}}_{O}$ = a mol; ${{n}_{{{N}_{2}}}}$ = b mol
$\to {{n}_{Z}}$ = a + b + 0,04 = 0,08; ${{m}_{Z}}=$ 44a + 28b + 0,04.2 = 0,08.20
Giải hệ có: a = 0,025 mol; b = 0,015 mol $\to \%{{m}_{{{N}_{2}}O}}=~~\dfrac{0,025.44}{1,6}.100\%=68,75\%.$
$\underbrace{\left\{ \begin{matrix}
Al \\
A{{l}_{2}}{{O}_{3}} \\
Al{{(N{{O}_{3}})}_{3}} \\
\end{matrix} \right\}}_{10,92(g)}+\left\{ \begin{matrix}
NaHS{{O}_{4}} \\
HN{{O}_{3}}:0,09 \\
\end{matrix} \right\}\to \left\{ \begin{matrix}
{{N}_{2}}O \\
{{N}_{2}} \\
{{H}_{2}} \\
\end{matrix} \right\}+{{H}_{2}}O+\left\{ \begin{matrix}
A{{l}^{3+}} \\
N{{a}^{+}} \\
NH_{4}^{+} \\
{{H}^{+}} \\
SO_{4}^{2-} \\
\end{matrix} \right\}$
Từ 1 mol NaOH đến 1,3 mol NaOH thì kết tủa từ cực đại đến tan hết do xảy ra phản ứng:
$Al{{(OH)}_{3}}+NaOH\to NaA1{{O}_{2}}+2{{H}_{2}}O\to {{n}_{A{{l}^{3+}}}}={{n}_{Al{{(OH)}_{3}}}}=1,3-1=0,3mol.$
Đặt ${{n}_{NaHS{{0}_{4}}}}=x\ mol\to {{n}_{N{{a}^{+}}/Y}}={{n}_{SO_{4}^{2-}}}=x\ mol.$
Khi kết tủa đạt cực đại thì chỉ thu được Na2SO4.
$\to {{n}_{N{{a}_{2}}S{{0}_{4}}}}=x\ mol\Rightarrow \sum{{{n}_{N{{a}^{+}}}}}=2x\to {{n}_{N{{a}^{+}}/Y}}=2x-1=x\Rightarrow x=1.$
Đặt ${{n}_{NH_{4}^{+}}}$ = y mol; ${{n}_{{{H}^{+}}}}$ = z mol. Bảo toàn điện tích: 0,3.3 +l + y+z=1.2
mmuối = 127,88(g) = 0,3 . 27 + 1 . 23 + 18y + z + 1 . 96
Giải hệ có: y = 0,04 mol; z = 0,06 mol. Bảo toàn khối lượng:
${{m}_{H20}}$ = 10,92 + 1 . 120 + 0,09 .63 - 127,88 - 0,08 .20 = 7,1 lg $\Rightarrow {{n}_{{{H}_{2}}O}}$ = 0,395 mol.
Bảo toàn nguyên tố hiđro: ${{n}_{{{H}_{2}}}}$ = (1 + 0,09 - 0,04 .4 - 0,06 - 0,395.2)/2 - 0,04 mol.
Đặt ${{n}_{{{N}_{2}}}}_{O}$ = a mol; ${{n}_{{{N}_{2}}}}$ = b mol
$\to {{n}_{Z}}$ = a + b + 0,04 = 0,08; ${{m}_{Z}}=$ 44a + 28b + 0,04.2 = 0,08.20
Giải hệ có: a = 0,025 mol; b = 0,015 mol $\to \%{{m}_{{{N}_{2}}O}}=~~\dfrac{0,025.44}{1,6}.100\%=68,75\%.$
Đáp án B.