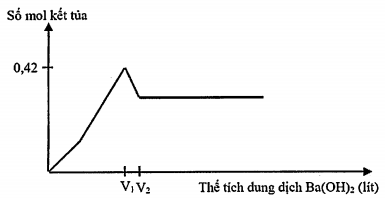
Câu hỏi: Cho từ từ dung dịch Ba(OH)2 1M đến dư vào 200 ml dung dịch chứa H2SO4 và Al2(SO4)3 xM. Phản ứng được biểu diễn theo đồ thị sau:
Biết ${{{V}_{2}}}/{{{V}_{1}}} =1,2$. Giá trị của x là
A. 0,3
B. 0,12
C. 0,06
D. 0,15
Biết ${{{V}_{2}}}/{{{V}_{1}}} =1,2$. Giá trị của x là

A. 0,3
B. 0,12
C. 0,06
D. 0,15
Đặt $a={{n}_{{{H}_{2}}S{{O}_{4}}}},b={{n}_{A{{l}_{2}}{{(S{{O}_{4}})}_{3}}}}$. Ta có ${{n}_{\downarrow \max }}=a+3b+2b=0,42$
Lại có ${{{V}_{2}}}/{{{V}_{1}}} =1,2$.
Ta có: ${{n}_{O{{H}^{-}}}}$ để tạo ra kết tủa cực đại $={{n}_{{{H}^{+}}}}+3{{n}_{A{{l}^{3+}}}}=2\text{a}+6b$.
${{n}_{O{{H}^{-}}}}$ để tạo ra kết tủa cực tiểu $={{n}_{{{H}^{+}}}}+4{{n}_{A{{l}^{3+}}}}=2\text{a}+8b$.
Lập tỉ lệ: $\dfrac{2\text{a}+8b}{2a+6b}=1,2\Rightarrow a=0,12\text{ mol}\text{, }b=0,06\text{ mol}$
$\Rightarrow x={b}/{0,2} =0,3$.
Lại có ${{{V}_{2}}}/{{{V}_{1}}} =1,2$.
Ta có: ${{n}_{O{{H}^{-}}}}$ để tạo ra kết tủa cực đại $={{n}_{{{H}^{+}}}}+3{{n}_{A{{l}^{3+}}}}=2\text{a}+6b$.
${{n}_{O{{H}^{-}}}}$ để tạo ra kết tủa cực tiểu $={{n}_{{{H}^{+}}}}+4{{n}_{A{{l}^{3+}}}}=2\text{a}+8b$.
Lập tỉ lệ: $\dfrac{2\text{a}+8b}{2a+6b}=1,2\Rightarrow a=0,12\text{ mol}\text{, }b=0,06\text{ mol}$
$\Rightarrow x={b}/{0,2} =0,3$.
Đáp án A.