Câu hỏi: Cho a mol P2O5 vào dung dịch chứa 3a mol KOH. Sau khi phản ứng xảy ra hoàn toàn, dung dịch thu được chứa các chất tan là:
A. H3PO4 và KH2PO4.
B. K3PO4 và KOH.
C. K3PO4 và K2HPO4.
D. K2HPO4 và KH2PO4
A. H3PO4 và KH2PO4.
B. K3PO4 và KOH.
C. K3PO4 và K2HPO4.
D. K2HPO4 và KH2PO4
Phương pháp:
Ban đầu P2O5 phản ứng với KOH tạo thành H3PO4 sau đó H3PO4 phản ứng với KOH.
Dạng bài H3PO4+ OH:
H3PO4 + OH + H2PO4- + H2O
H3PO4 + 2OH- → HPO42- + 2H2O
H3PO4 + 3OH -→ PO43- + 3H2O
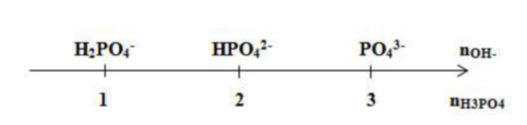
Giải thích trục số:
Đặt (*) $=\dfrac{{{n}_{O{{H}^{-}}}}}{{{n}_{{{H}_{2}}P{{O}_{4}}}}}$
+ Nếu (*) < 1 => H3PO4 dư và H2PO4 –
+ Nếu (*) = 1=> H2PO4 –
+ Nếu 1 < (*)< 2 $\Rightarrow $ H2PO4- và HPO42-
+ Nếu (*) = 2=> HPO42-
+ Nếu 2 < (*) < 3 => HPO42- và PO43-
+ Nếu (*) = 3 => PO43-
+ Nếu (*) > 3=> PO43- và OH dư
Hướng dẫn giải:
Ban đầu P2O5 phản ứng với KOH tạo thành H3PO4 sau đó H3PO4 phản ứng với KOH.
Bảo toàn $\to {{\text{n}}_{{{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}}}=2.{{\text{n}}_{{{P}_{2}}{{O}_{2}}}}=2\text{a}(\text{mol})$
Ta thấy:
$1<\dfrac{{{n}_{\text{KOH}}}}{{{n}_{{{H}_{2}}P{{O}_{4}}}}}=\dfrac{3a}{2a}=1,5<2$ nên tạo muối KH2PO4 và K2HPO4
Ban đầu P2O5 phản ứng với KOH tạo thành H3PO4 sau đó H3PO4 phản ứng với KOH.
Dạng bài H3PO4+ OH:
H3PO4 + OH + H2PO4- + H2O
H3PO4 + 2OH- → HPO42- + 2H2O
H3PO4 + 3OH -→ PO43- + 3H2O
Giải thích trục số:
Đặt (*) $=\dfrac{{{n}_{O{{H}^{-}}}}}{{{n}_{{{H}_{2}}P{{O}_{4}}}}}$
+ Nếu (*) < 1 => H3PO4 dư và H2PO4 –
+ Nếu (*) = 1=> H2PO4 –
+ Nếu 1 < (*)< 2 $\Rightarrow $ H2PO4- và HPO42-
+ Nếu (*) = 2=> HPO42-
+ Nếu 2 < (*) < 3 => HPO42- và PO43-
+ Nếu (*) = 3 => PO43-
+ Nếu (*) > 3=> PO43- và OH dư
Hướng dẫn giải:
Ban đầu P2O5 phản ứng với KOH tạo thành H3PO4 sau đó H3PO4 phản ứng với KOH.
Bảo toàn $\to {{\text{n}}_{{{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}}}=2.{{\text{n}}_{{{P}_{2}}{{O}_{2}}}}=2\text{a}(\text{mol})$
Ta thấy:
$1<\dfrac{{{n}_{\text{KOH}}}}{{{n}_{{{H}_{2}}P{{O}_{4}}}}}=\dfrac{3a}{2a}=1,5<2$ nên tạo muối KH2PO4 và K2HPO4
Đáp án D.