Câu hỏi: Thí nghiệm 1: Phản ứng giữa kim loại và dung dịch axit
- Tiến hành TN:
+ Cho vào ống nghiệm khoảng 2ml dd H2SO4 loãng
+ Bỏ thêm vào ống nghiệm 1 viên Zn nhỏ

- Hiện tượng: Phản ứng sủi bọt khí
- Giải thích: Zn tan trong axit H2SO4 sinh ra khí H2
PTHH: Zn + H2SO4 → ZnSO4 + H2
Zn: Chất khử
H2SO4: chất oxi hóa
Thí nghiệm 2: Phản ứng giữa kim loại và dung dịch muối
- Tiến hành TN:
+ Cho vào ống nghiệm khoảng 2ml CuSO4 loãng
+ Bỏ thêm 1 đinh sắt đã đánh sạch, để yên 10 phút
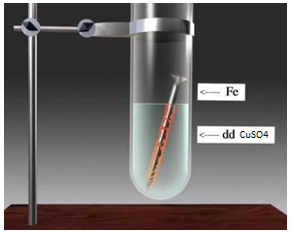
- Hiện tượng:
Đinh sắt tan, có lớp kim loại màu đỏ bám bên ngoài đinh sắt; màu xanh của dung dịch nhạt dần.
- Giải thích:
Vì Fe hoạt động mạnh hơn Cu nên Fe đã đẩy Cu ra khỏi muối CuSO4 tạo thành kim loại Cu có màu đỏ bám vào đinh sắt. Dung dịch CuSO4 có màu xanh lam khi phản ứng tạo muối FeSO4 nên màu xanh của dd nhạt dần.
PTHH: Fe + CuSO4 → FeSO4 + Cu
Fe : Chất khử
CuSO4: chất oxi hóa
Thí nghiệm 3: Phản ứng oxi hóa- khử giữa Mg và CO2
- Tiến hành TN:
+ Đốt cháy Mg trong không khí rồi bỏ vào bình chứa CO2 (đáy bình CO2 bỏ 1 ít cát để bảo vệ bình).
- Hiện tượng: Mg cháy tạo bột trắng và xuất hiện muội đen.
- Giải thích: ở điều kiện nhiệt độ, Mg đã phản ứng với CO2 tạo ra muội than (Cacbon) màu đen và MgO màu trắng.
PTHH: Mg + CO2 → MgO + C
Mg: Chất khử
CO2: Chất oxi hóa
Từ thí nghiệm trên ta thấy không thể dập tắt Mg đang cháy bằng bình phun CO2 vì Mg cháy trong CO2 làm cho đám cháy mạnh hơn.
Thí nghiệm 4: Phản ứng oxi hóa – khử trong môi trường axit
- Tiến hành TN:
+ Rót vào ống nghiệm 2ml dd FeSO4
+ Thêm vào đó 1ml dd H2SO4
+ Nhỏ từng giọt dd KMnO4 vào ống nghiệm, lắc nhẹ.
- Hiện tượng: Dd mất màu tím của KMnO4, xuất hiện muối màu đỏ nâu của Fe3+.
- Giải thích: KMnO4 là chất oxi hóa mạnh, có khả năng oxi hóa Fe2+ lên Fe3+ do đó làm mất màu thuốc tím.
PTHH: KMnO4 + 10FeSO4 + 7H2SO4 → 5Fe2(SO4)3 + K2SO4 + MnSO4 + 7H2O
KMnO4: Chất oxi hóa
FeSO4: Chất khử
- Tiến hành TN:
+ Cho vào ống nghiệm khoảng 2ml dd H2SO4 loãng
+ Bỏ thêm vào ống nghiệm 1 viên Zn nhỏ

- Hiện tượng: Phản ứng sủi bọt khí
- Giải thích: Zn tan trong axit H2SO4 sinh ra khí H2
PTHH: Zn + H2SO4 → ZnSO4 + H2
Zn: Chất khử
H2SO4: chất oxi hóa
Thí nghiệm 2: Phản ứng giữa kim loại và dung dịch muối
- Tiến hành TN:
+ Cho vào ống nghiệm khoảng 2ml CuSO4 loãng
+ Bỏ thêm 1 đinh sắt đã đánh sạch, để yên 10 phút

- Hiện tượng:
Đinh sắt tan, có lớp kim loại màu đỏ bám bên ngoài đinh sắt; màu xanh của dung dịch nhạt dần.
- Giải thích:
Vì Fe hoạt động mạnh hơn Cu nên Fe đã đẩy Cu ra khỏi muối CuSO4 tạo thành kim loại Cu có màu đỏ bám vào đinh sắt. Dung dịch CuSO4 có màu xanh lam khi phản ứng tạo muối FeSO4 nên màu xanh của dd nhạt dần.
PTHH: Fe + CuSO4 → FeSO4 + Cu
Fe : Chất khử
CuSO4: chất oxi hóa
Thí nghiệm 3: Phản ứng oxi hóa- khử giữa Mg và CO2
- Tiến hành TN:
+ Đốt cháy Mg trong không khí rồi bỏ vào bình chứa CO2 (đáy bình CO2 bỏ 1 ít cát để bảo vệ bình).
- Hiện tượng: Mg cháy tạo bột trắng và xuất hiện muội đen.
- Giải thích: ở điều kiện nhiệt độ, Mg đã phản ứng với CO2 tạo ra muội than (Cacbon) màu đen và MgO màu trắng.
PTHH: Mg + CO2 → MgO + C
Mg: Chất khử
CO2: Chất oxi hóa
Từ thí nghiệm trên ta thấy không thể dập tắt Mg đang cháy bằng bình phun CO2 vì Mg cháy trong CO2 làm cho đám cháy mạnh hơn.
Thí nghiệm 4: Phản ứng oxi hóa – khử trong môi trường axit
- Tiến hành TN:
+ Rót vào ống nghiệm 2ml dd FeSO4
+ Thêm vào đó 1ml dd H2SO4
+ Nhỏ từng giọt dd KMnO4 vào ống nghiệm, lắc nhẹ.
- Hiện tượng: Dd mất màu tím của KMnO4, xuất hiện muối màu đỏ nâu của Fe3+.
- Giải thích: KMnO4 là chất oxi hóa mạnh, có khả năng oxi hóa Fe2+ lên Fe3+ do đó làm mất màu thuốc tím.
PTHH: KMnO4 + 10FeSO4 + 7H2SO4 → 5Fe2(SO4)3 + K2SO4 + MnSO4 + 7H2O
KMnO4: Chất oxi hóa
FeSO4: Chất khử
Rất tiếc, câu hỏi này chưa có lời giải chi tiết. Bạn ơi, đăng nhập và giải chi tiết giúp zix.vn nhé!!!