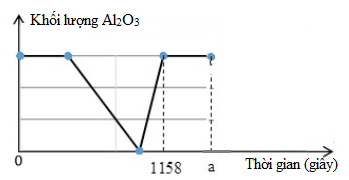
Câu hỏi: Điện phân dung dịch chứa x mol CuSO4, y mol H2SO4 và z mol NaCl (với điện cực trơ, màng ngăn xốp, hiệu suất điện phân là 100%, cường độ dòng điện không đổi I = 5A). Khối lượng Al2O3 bị hoà tan tối đa trong dung dịch sau điện phân phụ thuộc vào thời gian điện phân được biểu diễn trên đồ thị dưới đây:
Biết tại thời điểm 1158 giây và a giây khối lượng dung dịch điện phân giảm lần lượt là 2,81 gam và 3,17 gam. Giá trị của a là
A. 2316.
B. 1544.
C. 1930.
D. 3860.
Biết tại thời điểm 1158 giây và a giây khối lượng dung dịch điện phân giảm lần lượt là 2,81 gam và 3,17 gam. Giá trị của a là
A. 2316.
B. 1544.
C. 1930.
D. 3860.
Đoạn 1: CuSO4 + 2NaCl → Cu + Cl2 + Na2SO4
Đoạn 2: H2SO4 + 2NaCl → H2 + Cl2 + Na2SO4
Đoạn 3: 2H2O + 2NaCl → H2 + Cl2 + 2NaOH
Đoạn 4: Điện phân nước ở 2 điện cực, tạo H2, O2.
Đoạn 3 kết thúc lúc t = 1158 → ne = 0,06
Anot: nCl2 = 0,06/2 = 0,03
Trong khoảng thời gian từ 1158 đến a:
nH2O bị điện phân = (3,17 – 2,81)/18 = 0,02
→ nO2 = 0,01
ne = aI/F = 0,03.2 + 0,01.4 → a = 1930s
Đoạn 2: H2SO4 + 2NaCl → H2 + Cl2 + Na2SO4
Đoạn 3: 2H2O + 2NaCl → H2 + Cl2 + 2NaOH
Đoạn 4: Điện phân nước ở 2 điện cực, tạo H2, O2.
Đoạn 3 kết thúc lúc t = 1158 → ne = 0,06
Anot: nCl2 = 0,06/2 = 0,03
Trong khoảng thời gian từ 1158 đến a:
nH2O bị điện phân = (3,17 – 2,81)/18 = 0,02
→ nO2 = 0,01
ne = aI/F = 0,03.2 + 0,01.4 → a = 1930s
Đáp án C.