Câu hỏi: Điện phân 400 ml dung dịch X gồm KCl, HCl và CuCl2 0,02M (điện cực trơ, màng ngăn xốp) với cường độ dòng điện bằng I = 1,93A. Biết thể tích dung dịch không thay đổi trong quá trình điện phân, bỏ qua sự thủy phân của ion Cu2+. Cho đồ thị biểu diễn mối quan hệ giữa thời gian điện phân và pH của dung dịch như hình vẽ:
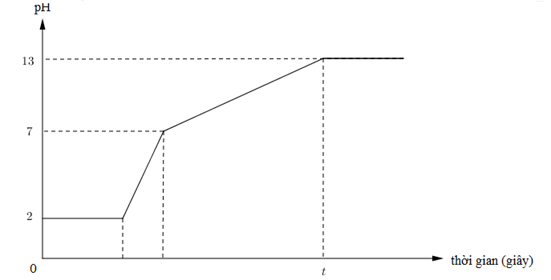
Phát biểu nào sau đây sai?
A. Nồng độ của HCl trong X là 0,01 M.
B. Giá trị t là 3000.
C. Thứ tự điện phân ở catot lần lượt là Cu2+, H+, H2O.
D. Khi thời gian điện phân là 600 giây, khối lượng kim loại ở catot là 0,512 gam.

Phát biểu nào sau đây sai?
A. Nồng độ của HCl trong X là 0,01 M.
B. Giá trị t là 3000.
C. Thứ tự điện phân ở catot lần lượt là Cu2+, H+, H2O.
D. Khi thời gian điện phân là 600 giây, khối lượng kim loại ở catot là 0,512 gam.
${{n}_{CuC{{l}_{2}}}}=0,008$
Ban đầu: $pH=2\to \left[ {{H}^{+}} \right]=0,01\to {{n}_{HCl}}=0,004$
$\to $ A đúng.
Đoạn 1:pH không thay đổi trong khoảng thời gian catot khử $C{{u}^{2+}}$ và anot oxi hóa $C{{l}^{-}}$.
${{n}_{e}}$ đoạn 1 $=2{{n}_{C{{u}^{2+}}}}=0,016$
Đoạn 2:pH tăng nhanh chóng do ${{H}^{+}}$ bị khử cho tới khi hết tại catot.
${{n}_{e}}$ đoạn 2 $={{n}_{{{H}^{+}}}}=0,004$
Đoạn 3: pH tiếp tục tăng, dung dịch chuyển sang môi trường kiềm do H2O bị khử tại catot tạo $O{{H}^{-}}:$
$pH=13\to \left[ O{{H}^{-}} \right]=0,1\to {{n}_{O{{H}^{-}}}}=0,04$
$2{{H}_{2}}O+2e\to 2O{{H}^{-}}+{{H}_{2}}$
$\to {{n}_{e}}$ đoạn 3 $={{n}_{O{{H}^{-}}}}=0,04$
${{n}_{e}}$ tổng 3 đoạn $=0,06=\dfrac{Ix}{F}$
$\to x=3000$ (B đúng)
C. Đúng
D. Sai
Khi $t=600s$ thì ${{n}_{e}}=\dfrac{It}{F}=0,012\to {{n}_{Cu}}=0,006$
$\to {{m}_{Cu}}=0,384$ gam
Ban đầu: $pH=2\to \left[ {{H}^{+}} \right]=0,01\to {{n}_{HCl}}=0,004$
$\to $ A đúng.
Đoạn 1:pH không thay đổi trong khoảng thời gian catot khử $C{{u}^{2+}}$ và anot oxi hóa $C{{l}^{-}}$.
${{n}_{e}}$ đoạn 1 $=2{{n}_{C{{u}^{2+}}}}=0,016$
Đoạn 2:pH tăng nhanh chóng do ${{H}^{+}}$ bị khử cho tới khi hết tại catot.
${{n}_{e}}$ đoạn 2 $={{n}_{{{H}^{+}}}}=0,004$
Đoạn 3: pH tiếp tục tăng, dung dịch chuyển sang môi trường kiềm do H2O bị khử tại catot tạo $O{{H}^{-}}:$
$pH=13\to \left[ O{{H}^{-}} \right]=0,1\to {{n}_{O{{H}^{-}}}}=0,04$
$2{{H}_{2}}O+2e\to 2O{{H}^{-}}+{{H}_{2}}$
$\to {{n}_{e}}$ đoạn 3 $={{n}_{O{{H}^{-}}}}=0,04$
${{n}_{e}}$ tổng 3 đoạn $=0,06=\dfrac{Ix}{F}$
$\to x=3000$ (B đúng)
C. Đúng
D. Sai
Khi $t=600s$ thì ${{n}_{e}}=\dfrac{It}{F}=0,012\to {{n}_{Cu}}=0,006$
$\to {{m}_{Cu}}=0,384$ gam
Đáp án D.