Câu hỏi: Cho 13,5g nhôm tác dụng vừa đủ với 2,2 lít dung dịch \(HN{O_3}\) phản ứng tạo ra muối nhôm và một hỗn hợp khí gồm \(NO\) và \({N_2}O\). Tính nồng độ mol của dung dịch \(HN{O_3}\). Biết rằng tỉ khối của hỗn hợp khí đối với hiđro bằng 19,2.
Lời giải chi tiết
Đặt số mol Al tham gia phản ứng (1) và (2) lần lượt là x mol và y mol.
\(\Rightarrow x + y = \frac{{13,5}}{{27}}\) (*)
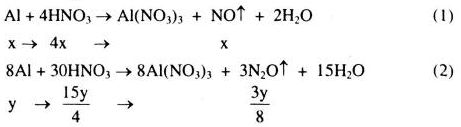
Hỗn hợp khí X gồm NO x mol: \({N_2}O \frac{{3y}}{8}\)mol
Theo đề bài ta có:
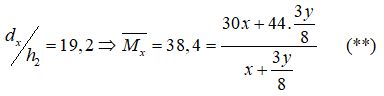
Giải hệ (*) và (**) ta được \(\left\{ \begin{array}{l}x = 0,1\\y = 0,4\end{array} \right.\)
Từ (1) và (2) \(\Rightarrow {n_{HN{O_3}}} = 4x + \frac{{15y}}{4} = 1,9\)mol
Nồng độ mol/lít của dung dịch \(HN{O_3}\) đã dùng:
\({CM_{{{HN{O_3}}}}} = \frac{{1,9}}{{2,2}} = 0,86M\)
Đặt số mol Al tham gia phản ứng (1) và (2) lần lượt là x mol và y mol.
\(\Rightarrow x + y = \frac{{13,5}}{{27}}\) (*)
Hỗn hợp khí X gồm NO x mol: \({N_2}O \frac{{3y}}{8}\)mol
Theo đề bài ta có:
Giải hệ (*) và (**) ta được \(\left\{ \begin{array}{l}x = 0,1\\y = 0,4\end{array} \right.\)
Từ (1) và (2) \(\Rightarrow {n_{HN{O_3}}} = 4x + \frac{{15y}}{4} = 1,9\)mol
Nồng độ mol/lít của dung dịch \(HN{O_3}\) đã dùng:
\({CM_{{{HN{O_3}}}}} = \frac{{1,9}}{{2,2}} = 0,86M\)