Câu hỏi: Đưa một bình cầu đựng 250 gam nước clo ra ngoài ánh sáng mặt trời thì có 0,112 lít (đktc) khí được giải phóng. Hỏi khí nào được giải phóng? Tính nồng độ % của clo trong dung dịch đầu, cho rằng tất cả clo tan trong nước, đã phản ứng với nước.
Phương pháp giải
Khí được giải phóng là \(O_2\). Tính toán theo PTHH
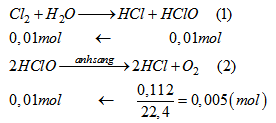
Lời giải chi tiết
Khí được giải phóng là \(O_2\)
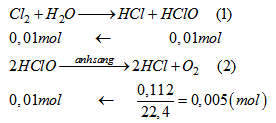
Từ (1) và (2) suy ra:
\(\begin{array}{l}
{n_{C{l_2}}} = 0,01\left({mol} \right)\\
C{\% _{\left({Clo} \right)}} = \dfrac{{71.0,01}}{{250}}. 100\% = 0,284\%
\end{array}\)
Khí được giải phóng là \(O_2\). Tính toán theo PTHH
Lời giải chi tiết
Khí được giải phóng là \(O_2\)
Từ (1) và (2) suy ra:
\(\begin{array}{l}
{n_{C{l_2}}} = 0,01\left({mol} \right)\\
C{\% _{\left({Clo} \right)}} = \dfrac{{71.0,01}}{{250}}. 100\% = 0,284\%
\end{array}\)