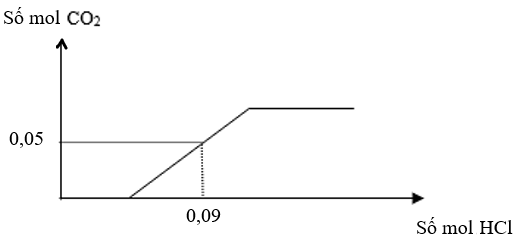
Câu hỏi: Dẫn 0,45 mol hỗn hợp gồm khí CO2 và hơi nước qua cacbon nung đỏ thu được 0,65 mol hỗn hợp X gồm CO, H2 và CO2. Cho toàn bộ X vào dung dịch chứa 0,1 mol NaOH và a mol Ba(OH)2, sau phản ứng hoàn toàn thu được kết tủa và dung dịch Y. Cho từ từ dung dịch HCl vào Y, sự phụ thuộc số mol khí CO2 và số mol HCl được biểu diễn theo đồ thị sau:
Giá trị của a là
A. 0,25.
B. 0,19.
C. 0,20.
D. 0,21.
Giá trị của a là
A. 0,25.
B. 0,19.
C. 0,20.
D. 0,21.
nC phản ứng = 0,65 – 0,45 = 0,2
Bảo toàn electron: 4nC phản ứng = 2nCO + $2{{n}_{{{H}_{2}}}}$
nCO + ${{n}_{{{H}_{2}}}}$ = 0,4 ${{n}_{C{{O}_{2}}}}$ = 0,65 – 0,4 = 0,25 mol
Cho HCl vào Y một thời gian mới có khí nên Y chứa CO32- Y không chứa Ba2+.
Mặt khác nHCl < 2 ${{n}_{C{{O}_{2}}}}$ nên Y không chứa OH-.
Y chứa Na2CO3 (x) và NaHCO3 (y)
Bảo toàn Na: 2x + y = 0,1 và nHCl = x + 0,05 = 0,09
x = 0,04; y = 0,02
Bảo toàn C: ${{n}_{BaC{{O}_{3}}}}$ = 0,25 – (x + y) = 0,19 a = 0,19.
Bảo toàn electron: 4nC phản ứng = 2nCO + $2{{n}_{{{H}_{2}}}}$
nCO + ${{n}_{{{H}_{2}}}}$ = 0,4 ${{n}_{C{{O}_{2}}}}$ = 0,65 – 0,4 = 0,25 mol
Cho HCl vào Y một thời gian mới có khí nên Y chứa CO32- Y không chứa Ba2+.
Mặt khác nHCl < 2 ${{n}_{C{{O}_{2}}}}$ nên Y không chứa OH-.
Y chứa Na2CO3 (x) và NaHCO3 (y)
Bảo toàn Na: 2x + y = 0,1 và nHCl = x + 0,05 = 0,09
x = 0,04; y = 0,02
Bảo toàn C: ${{n}_{BaC{{O}_{3}}}}$ = 0,25 – (x + y) = 0,19 a = 0,19.
Đáp án B.