Câu hỏi: Khi nhỏ từ từ đến dư dung dịch HCl vào dung dịch hỗn hợp gồm x mol Ba(OH)2 và y mol Ba[Al(OH)4]2 hoặc Ba(AlO2)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
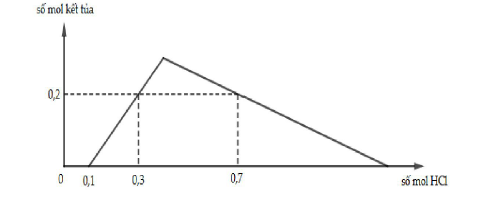
Giá trị của x và y lần lượt là
A. 0,10 và 0,15.
B. 0,10 và 0,30.
C. 0,05 và 0,15.
D. 0,05 và 0,30.

Giá trị của x và y lần lượt là
A. 0,10 và 0,15.
B. 0,10 và 0,30.
C. 0,05 và 0,15.
D. 0,05 và 0,30.
Phương pháp:
Bài toán đồ thị cho từ từ H+vào {OH-, AlO2-}
Thứ tự phản ứng khi cho từ từ ${{\text{H}}^{+}}\text{v }\!\!\grave{\mathrm{a}}\!\!\text{ o O}{{\text{H}}^{-}};\text{Al}{{\text{O}}_{2}}^{-}$ là:
(1) ${{\text{H}}^{+}}+\text{O}{{\text{H}}^{-}}\to {{\text{H}}_{2}}\text{O}$
(2) ${{\text{H}}^{+}}+\text{AlO}{{_{2}^{{}}}^{-}}+{{\text{H}}_{2}}\text{O}\to \text{Al}{{(\text{OH})}_{3}}$
(3) $3{{\text{H}}^{+}}+\text{Al}{{(\text{OH})}_{3}}\to \text{A}{{\text{l}}^{3+}}+3{{\text{H}}_{2}}\text{O}$
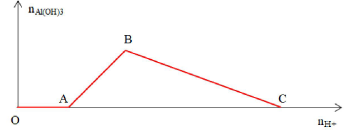
* Đoạn OA ứng với phản ứng (1)
* Đoạn AB ứng với phản ứng (2)
* Đoạn BC ứng với phản ứng (3)
Xét 2 điểm sau:
1. Điểm thuộc đoạn AB: kết tủa chưa đạt cực đại
${{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{H}+(1)}}+{{\text{n}}_{\text{H}+(2)}}\text{ hay }{{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{OH}}}_{\text{-}}+{{\text{n}}_{\text{Al}{{(\text{OH})}_{^{3}}}}}$
2. Điểm thuộc đoạn BC: kết tủa tan một phần
${{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{H}+(1)}}+{{\text{n}}_{\text{H}+(2)}}\max +{{\text{n}}_{\text{H}+(3)}}={{\text{n}}_{\text{OH}-}}+{{\text{n}}_{\text{AlO}2-(\text{bd})}}+3{{\text{n}}_{\text{Al}(\text{OH})3}}$ bị tan (*)
Mà bảo toàn Al→ nAl(OH)3 bị tan = nAlO2-(bđ) - nAl(OH)3
Thay vào (*) → nH+= nOH- + 4nAlO2-(bđ) - 3nAl(OH)3
Hướng dẫn giải:
Dung dịch ban đầu có: ${{\text{n}}_{\text{O}{{\text{H}}^{-}}}}=2\text{x mol v }\!\!\grave{\mathrm{a}}\!\!\text{ }{{\text{n}}_{\text{AlO}{{2}^{-}}}}=2\text{y mol}$
- Khi nHCl = 0,1 mol:
${{\text{n}}_{{{\text{H}}^{+}}}}={{n}_{OH-}}=0,1\to 2\text{x}=0,1\to \text{x}=0,05$
- Khi nHCl = 0,7 mol:
${{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{OH}-}}+4{{\text{n}}_{\text{A}1\text{O}2-}}-3{{\text{n}}_{\text{Al}(\text{OH})3}}\to 0,7=0,1+4.2\text{y}-3.0,2\to $ y = 0,15
Bài toán đồ thị cho từ từ H+vào {OH-, AlO2-}
Thứ tự phản ứng khi cho từ từ ${{\text{H}}^{+}}\text{v }\!\!\grave{\mathrm{a}}\!\!\text{ o O}{{\text{H}}^{-}};\text{Al}{{\text{O}}_{2}}^{-}$ là:
(1) ${{\text{H}}^{+}}+\text{O}{{\text{H}}^{-}}\to {{\text{H}}_{2}}\text{O}$
(2) ${{\text{H}}^{+}}+\text{AlO}{{_{2}^{{}}}^{-}}+{{\text{H}}_{2}}\text{O}\to \text{Al}{{(\text{OH})}_{3}}$
(3) $3{{\text{H}}^{+}}+\text{Al}{{(\text{OH})}_{3}}\to \text{A}{{\text{l}}^{3+}}+3{{\text{H}}_{2}}\text{O}$
* Đoạn OA ứng với phản ứng (1)
* Đoạn AB ứng với phản ứng (2)
* Đoạn BC ứng với phản ứng (3)
Xét 2 điểm sau:
1. Điểm thuộc đoạn AB: kết tủa chưa đạt cực đại
${{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{H}+(1)}}+{{\text{n}}_{\text{H}+(2)}}\text{ hay }{{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{OH}}}_{\text{-}}+{{\text{n}}_{\text{Al}{{(\text{OH})}_{^{3}}}}}$
2. Điểm thuộc đoạn BC: kết tủa tan một phần
${{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{H}+(1)}}+{{\text{n}}_{\text{H}+(2)}}\max +{{\text{n}}_{\text{H}+(3)}}={{\text{n}}_{\text{OH}-}}+{{\text{n}}_{\text{AlO}2-(\text{bd})}}+3{{\text{n}}_{\text{Al}(\text{OH})3}}$ bị tan (*)
Mà bảo toàn Al→ nAl(OH)3 bị tan = nAlO2-(bđ) - nAl(OH)3
Thay vào (*) → nH+= nOH- + 4nAlO2-(bđ) - 3nAl(OH)3
Hướng dẫn giải:
Dung dịch ban đầu có: ${{\text{n}}_{\text{O}{{\text{H}}^{-}}}}=2\text{x mol v }\!\!\grave{\mathrm{a}}\!\!\text{ }{{\text{n}}_{\text{AlO}{{2}^{-}}}}=2\text{y mol}$
- Khi nHCl = 0,1 mol:
${{\text{n}}_{{{\text{H}}^{+}}}}={{n}_{OH-}}=0,1\to 2\text{x}=0,1\to \text{x}=0,05$
- Khi nHCl = 0,7 mol:
${{\text{n}}_{\text{H}+}}={{\text{n}}_{\text{OH}-}}+4{{\text{n}}_{\text{A}1\text{O}2-}}-3{{\text{n}}_{\text{Al}(\text{OH})3}}\to 0,7=0,1+4.2\text{y}-3.0,2\to $ y = 0,15
Đáp án C.